Carbons elektronaffinitet:Forståelse af valenselektroner
Her er hvorfor:
* Atomstruktur: Kulstof har i alt 6 elektroner. Dens elektronkonfiguration er 2, 4. Det betyder, at den har 2 elektroner i sin første skal og 4 elektroner i sin anden skal.
* Oktetregel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af 8 elektroner i deres yderste skal (oktetreglen).
* Kulstofmål: Kulstof har kun 4 elektroner i sin ydre skal. For at opnå stabilitet ønsker den at få 4 elektroner mere, hvilket bringer dets samlede antal til 8.
Det er derfor, kulstof danner fire bindinger, ofte med andre kulstofatomer eller med atomer som brint, oxygen og nitrogen.
 Varme artikler
Varme artikler
-
 Ser mod solen for at skabe brintbrændstofEn kunstnerisk gengivelse af grænsefladen mellem et fotoabsorberende materiale og en vandig elektrolyt. Kredit:Lawrence Livermore National Laboratory Da Lawrence Livermore-forskeren Tadashi Ogitsu
Ser mod solen for at skabe brintbrændstofEn kunstnerisk gengivelse af grænsefladen mellem et fotoabsorberende materiale og en vandig elektrolyt. Kredit:Lawrence Livermore National Laboratory Da Lawrence Livermore-forskeren Tadashi Ogitsu -
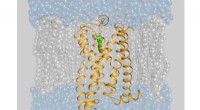 Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f
Farmakonutrition:Moderne lægemiddeldesign til funktionelle undersøgelserModel af den bitre receptor TAS2R14 med en af dens aktivatorer (ligander), flufenaminsyren. Kredit:Antonella Di Pizio/Leibniz-LSB@TUM Antonella Di Pizio og Maik Behrens fra Leibniz-instituttet f -
 Datadeling er fremtiden for materialeforskningKredit: Avanceret Videnskab Brug af data til at designe og udvikle helt nye materialer er et hastigt voksende videnskabsområde. En gruppe forskere ved Aalto-universitetet har netop offentliggjort
Datadeling er fremtiden for materialeforskningKredit: Avanceret Videnskab Brug af data til at designe og udvikle helt nye materialer er et hastigt voksende videnskabsområde. En gruppe forskere ved Aalto-universitetet har netop offentliggjort -
 Elektriske vandpiber er måske ikke sikrere end traditionelle kul-baseredeKredit:American Chemical Society Vandpibetobaksrygning, ellers kendt som vandpibe eller shisha, bliver stadig mere populær over hele verden, især blandt unge. Traditionelle vandpiber brænder træk
Elektriske vandpiber er måske ikke sikrere end traditionelle kul-baseredeKredit:American Chemical Society Vandpibetobaksrygning, ellers kendt som vandpibe eller shisha, bliver stadig mere populær over hele verden, især blandt unge. Traditionelle vandpiber brænder træk
- Hvordan er bakterierne og archaea forskellige fra alle andre cellulære mikrober?
- Er streaming af video fra skitserede websteder ulovligt?
- Er faren for identitetstyveri overdreven?
- At forsvinde guld er en velsignelse for nanogittere
- Hvem skabte og byggede Hubble-teleskopet?
- Hvad er det forholdet mellem temperatur og lysstyrke af stjerner?


