Natriumbisulfit pH:Forståelse af surhed og hydrolyse
Her er hvorfor:
* Hydrolyse: Når natriumbisulfit opløses i vand, undergår det hydrolyse og danner bisulfitioner (HSO₃⁻) og natriumioner (Na⁺). Bisulfitionerne kan donere en proton (H⁺) til vand, hvilket gør opløsningen sur:
```
HSO3⁻ + H₂O⇌ SO₃²⁻ + H3O⁺
```
* Ligevægt: Ligevægten ligger til højre, hvilket betyder, at flere bisulfitioner donerer protoner, hvilket øger koncentrationen af hydroniumioner (H₃O⁺) og sænker pH.
Vigtige bemærkninger:
* Koncentration: Den nøjagtige pH af en natriumbisulfitopløsning afhænger af dens koncentration. En mere koncentreret opløsning vil være mere sur.
* Temperatur: Temperaturen påvirker også pH. En højere temperatur vil begunstige produktionen af H₃O⁺, hvilket gør opløsningen mere sur.
Sig til, hvis du har andre spørgsmål!
Sidste artikelMolekyler:definition, struktur og typer | Kemi forklaret
Næste artikelKaliumoxid (K₂O):Forståelse af atomsammensætning
 Varme artikler
Varme artikler
-
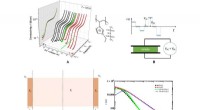 Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel
Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel -
 Undersøgelse af elefant, capybara, menneskehår finder ud af, at tykkere hår ikke altid er stærke…Billedet viser, hvordan proteinfibre i menneskehårets cortex delaminerer, når håret går i stykker, tyder på brud på menneskehår i forskydningstilstand. Kredit:Wen Yang På trods af at være fire gan
Undersøgelse af elefant, capybara, menneskehår finder ud af, at tykkere hår ikke altid er stærke…Billedet viser, hvordan proteinfibre i menneskehårets cortex delaminerer, når håret går i stykker, tyder på brud på menneskehår i forskydningstilstand. Kredit:Wen Yang På trods af at være fire gan -
 Kører på tom:Ny overkommelig katalysator er afhængig af ledige nitrogenpladser til at producere a…Nikkelbelastet lanthannitrid (LaN) muliggør stabil og yderst effektiv ammoniaksyntese. Kvælstofplaceringer genereres på LaN med lav formationsenergi, og effektivt binde og aktivere N2. Kredit:Tokyo Te
Kører på tom:Ny overkommelig katalysator er afhængig af ledige nitrogenpladser til at producere a…Nikkelbelastet lanthannitrid (LaN) muliggør stabil og yderst effektiv ammoniaksyntese. Kvælstofplaceringer genereres på LaN med lav formationsenergi, og effektivt binde og aktivere N2. Kredit:Tokyo Te -
 Hydrodynamik i cellestudierKredit:IBM I samarbejde med ETH Zürich, vores team hos IBM Research – Zurich udgav en artikel, der gennemgår interaktionen mellem væskestrømme og biologiske celler. Vores arbejde blev vist på fors
Hydrodynamik i cellestudierKredit:IBM I samarbejde med ETH Zürich, vores team hos IBM Research – Zurich udgav en artikel, der gennemgår interaktionen mellem væskestrømme og biologiske celler. Vores arbejde blev vist på fors


