Kaliumchloratopløselighed:Metoder og temperaturdata
1. Brug af opløselighedstabeller:
* Slå det op: Opløselighedstabeller er let tilgængelige online eller i kemi lærebøger. De giver opløseligheden af forskellige forbindelser ved forskellige temperaturer.
* Eksempel: En typisk opløselighedstabel vil vise opløseligheden af KClO3 i gram pr. 100 g vand ved forskellige temperaturer. For eksempel ved 20°C er opløseligheden af KClO3 ca. 7,4 g pr. 100 g vand.
2. Eksperimentel bestemmelse af opløselighed:
* Mættet løsning:
* Forbered: Tilsæt en kendt mængde KClO3 til en kendt mængde vand ved en bestemt temperatur.
* Rør: Rør blandingen kraftigt, indtil der ikke er mere KClO3 opløst. Dette er en mættet løsning.
* Filter: Filtrer opløsningen for at fjerne eventuel uopløst KClO3.
* Fordamp: Fordamp forsigtigt vandet fra filtratet. Det resterende faste stof er det opløste KClO3.
* Beregn: Mål massen af det tørrede KClO3. Divider denne masse med det oprindelige volumen vand, der blev brugt til at bestemme opløseligheden i g pr. 100 g vand.
3. Brug af en opløselighedskurve:
* Plotopløselighed: En opløselighedskurve viser forholdet mellem temperatur og opløselighed for en given forbindelse. Du kan finde disse kurver online eller i kemiressourcer.
* Find opløselighed: Find den temperatur, du er interesseret i, på x-aksen. Følg kurven, der repræsenterer KClO3 lodret for at finde den tilsvarende opløselighed på y-aksen.
Vigtige overvejelser:
* Temperatur: Opløseligheden af de fleste faste stoffer stiger med temperaturen.
* Tryk: Tryk har en minimal effekt på opløseligheden af faste stoffer, men det kan betydeligt påvirke opløseligheden af gasser.
* Enheder: Opløselighed udtrykkes normalt i gram opløst stof pr. 100 gram opløsningsmiddel (g/100g), men der anvendes også andre enheder, såsom molaritet (mol/L).
Fortæl mig, hvis du har en bestemt temperatur eller et scenarie i tankerne, så kan jeg hjælpe dig med at bestemme opløseligheden af kaliumchlorat!
 Varme artikler
Varme artikler
-
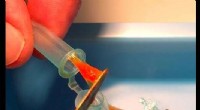 Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky -
 Beregn nemt Square Yards:En hurtig, praktisk vejledningAf Lisa Maloney Opdateret 24. marts 2022 Hvis du bor i USA eller Storbritannien, kan du støde på en måling kendt som square yard. (I andre dele af verden vil du være meget mere tilbøjelig til at st
Beregn nemt Square Yards:En hurtig, praktisk vejledningAf Lisa Maloney Opdateret 24. marts 2022 Hvis du bor i USA eller Storbritannien, kan du støde på en måling kendt som square yard. (I andre dele af verden vil du være meget mere tilbøjelig til at st -
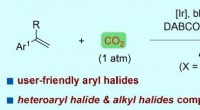 Synligt lys-drevet arylcarboxylering af styrener med kuldioxid og arylhalogeniderFigur:Synligt lys-drevet arylcarboxylering af styrener med CO2 og arylhalogenider. Kredit:Prof. LIs gruppe Brugen af kuldioxid (CO 2 ), som er en ideel one-carbon (C1) byggesten og er bæredygt
Synligt lys-drevet arylcarboxylering af styrener med kuldioxid og arylhalogeniderFigur:Synligt lys-drevet arylcarboxylering af styrener med CO2 og arylhalogenider. Kredit:Prof. LIs gruppe Brugen af kuldioxid (CO 2 ), som er en ideel one-carbon (C1) byggesten og er bæredygt -
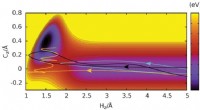 Forskere finder, at H-C-bindinger dannes, når brintatomer kolliderer med grafen med høj hastighedRehybridisering i dannelsen af en C-H-binding ved kollisioner af et H-atom på en grafenoverflade. HZ og CZ er afstandene mellem H- og C -atomerne fra grafenplanet. Tre baner er vist for H-atomer med
Forskere finder, at H-C-bindinger dannes, når brintatomer kolliderer med grafen med høj hastighedRehybridisering i dannelsen af en C-H-binding ved kollisioner af et H-atom på en grafenoverflade. HZ og CZ er afstandene mellem H- og C -atomerne fra grafenplanet. Tre baner er vist for H-atomer med


