Hydrogen vs. Deuterium-reaktioner:Forstå forskellen
* Kinetisk isotopeffekt: Denne effekt opstår som følge af forskellen i masse mellem brint (protium, ¹H) og deuterium (²H). Deuterium er omkring dobbelt så tungt som brint.
* Nulpunktsenergi: Kvantemekanikken dikterer, at selv ved det absolutte nulpunkt har molekyler en vis vibrationsenergi, kaldet nulpunktsenergi. Lettere isotoper har højere nulpunktsenergi, hvilket betyder, at de vibrerer hurtigere.
* Aktiveringsenergi: Reaktioner kræver energi for at overvinde en aktiveringsbarriere. Brintens højere nulpunktsenergi gør det lettere at nå aktiveringsenergien og reagere hurtigere.
Eksempel: Overvej en simpel reaktion som forbrænding af brint og deuterium med oxygen:
* H2 + ½O2 → H2O
* D2 + ½O2 → D2O
Reaktionen med hydrogen (H2) vil forløbe hurtigere end reaktionen med deuterium (D2). Dette skyldes, at aktiveringsenergien for reaktionen med brint er lavere på grund af dens højere nulpunktsenergi.
Bemærk: Den kinetiske isotopeffekt kan være betydelig, men det er ikke altid den dominerende faktor. Andre faktorer som steriske effekter og reaktionens art kan også spille en rolle i reaktionshastigheder.
Sidste artikelSyreaflejring:3 store indvirkninger på miljø og sundhed
Næste artikelAtomer i SiO:Forståelse af siliciummonoxidsammensætning
 Varme artikler
Varme artikler
-
 Farmakoskopi muliggør opdagelse af immunmodulerende lægemidler ved at analysere immuncelleinterakt…Gregory Vladimer, Nikolaus Krall, Berend Snijder og Giulio Superti-Furga (fra venstre mod højre) er ved siden af Pharmacoscopy high-throughput mikroskop. Kredit:Wolfgang Däuble/CeMM Immunsysteme
Farmakoskopi muliggør opdagelse af immunmodulerende lægemidler ved at analysere immuncelleinterakt…Gregory Vladimer, Nikolaus Krall, Berend Snijder og Giulio Superti-Furga (fra venstre mod højre) er ved siden af Pharmacoscopy high-throughput mikroskop. Kredit:Wolfgang Däuble/CeMM Immunsysteme -
 Lab-lavet hormon kan afsløre planters hemmelige livEn syntetisk version af auxin og dets proteinreceptor (lyseblå) lægger sig sammen, skabe et konstrueret par, der opfører sig ligesom det naturlige. Kredit:Keiko Torii/University of Washington/Howard H
Lab-lavet hormon kan afsløre planters hemmelige livEn syntetisk version af auxin og dets proteinreceptor (lyseblå) lægger sig sammen, skabe et konstrueret par, der opfører sig ligesom det naturlige. Kredit:Keiko Torii/University of Washington/Howard H -
 Stigende temperaturer Lavere relativ luftfugtighed:hvorfor det betyder nogettaniche/iStock/GettyImages Meteorologer anvender en række metrikker til at kvantificere atmosfærisk fugt. Blandt disse relativ fugtighed (RH) er altafgørende, fordi det direkte har indflydelse på, hv
Stigende temperaturer Lavere relativ luftfugtighed:hvorfor det betyder nogettaniche/iStock/GettyImages Meteorologer anvender en række metrikker til at kvantificere atmosfærisk fugt. Blandt disse relativ fugtighed (RH) er altafgørende, fordi det direkte har indflydelse på, hv -
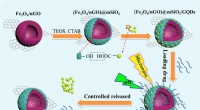 N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk
N-dopede carbonindkapslede overgangsmetalkatalysatorer for at optimere ydeevnen af zink-luftbatter…Fe@NCG blev fremstillet ved pyrolysering af opløsningsmiddelfri dannede Fechitosan-chelater og yderligere nitrogen-urinstof med lille molekyle. Den dannede katalysator udviser bifunktionel katalytisk
- Hvor mange bjerge på jorden er højere end 8000 meter?
- Ville dagslys besparelser være nyttige for Antarktis?
- In-situ måling af 3-D proteinstruktur inde i levende eukaryote celler
- 'The boss of Country', ikke vilde hunde at dræbe:Hvordan det at leve med dingoer kan forene samfund…
- Er en bordsaltforbindelse af natrium og klor sand eller falsk?
- UH-professor tager næste skridt med grafenforskning


