Ionbinding:Hvordan modsat ladede ioner skaber kemiske bindinger
1. Dannelse af ioner:
* Metaller har en tendens til at miste elektroner for at opnå en stabil elektronkonfiguration og bliver til positivt ladede kationer .
* Ikke-metaller har tendens til at få elektroner for at opnå en stabil elektronkonfiguration og bliver negativt ladede anioner .
2. Elektrostatisk tiltrækning:
* Modsatte afgifter tiltrækker. Når en kation (positiv) og en anion (negativ) bringes tæt sammen, udøver deres modsatte ladninger en stærk elektrostatisk tiltrækningskraft.
3. Dannelse af den ioniske binding:
* Denne elektrostatiske tiltrækning holder ionerne sammen og danner en kemisk binding kaldet en ionisk binding .
* Den resulterende forbindelse kaldes en ionisk forbindelse eller salt .
Eksempel:Natriumchlorid (NaCl)
* Natrium (Na) mister en elektron for at blive en positivt ladet natriumion (Na+).
* Klor (Cl) får en elektron til at blive en negativt ladet chloridion (Cl-).
* De modsatte ladninger tiltrækker og danner en ionbinding mellem Na+ og Cl- ionerne, hvilket skaber natriumchlorid (NaCl), som er bordsalt.
Nøglekarakteristika for ioniske bindinger:
* Stærk attraktion: Ionbindinger er relativt stærke, hvilket resulterer i høje smelte- og kogepunkter.
* Krystallinsk struktur: Ioniske forbindelser danner typisk en stiv, krystallinsk struktur.
* Opløselighed: Mange ioniske forbindelser er opløselige i vand, fordi de polære vandmolekyler kan omgive og adskille ionerne.
* Konduktivitet: Ioniske forbindelser leder elektricitet, når de opløses i vand eller smeltes, da de fritgående ioner kan føre elektrisk strøm.
Opsummering:
Modsat ladede ioner tiltrækker hinanden på grund af elektrostatiske kræfter og danner ionbindinger. Disse bindinger holder ionerne sammen i en stiv, krystallinsk struktur, hvilket skaber ioniske forbindelser.
Sidste artikelIoniske bindinger:Forstå tiltrækningen mellem ioner
Næste artikelKovalente forbindelser og kationer:Forstå forskellen
 Varme artikler
Varme artikler
-
 Photopower til mikrolabsKredit:Wiley-VCH Miniaturiserede enheder såsom mikrosensorer kræver ofte en uafhængig, lige så miniaturiseret strømforsyning. Søger efter passende systemer, Japanske videnskabsmænd har nu udviklet
Photopower til mikrolabsKredit:Wiley-VCH Miniaturiserede enheder såsom mikrosensorer kræver ofte en uafhængig, lige så miniaturiseret strømforsyning. Søger efter passende systemer, Japanske videnskabsmænd har nu udviklet -
 En lavtemperaturmetode til fremstilling af højtydende termoelektriske materialerMohamad Nugraha (til venstre) og hans gruppeleder, Derya Baran, demonstrere enhedens fleksibilitet. Kredit:KAUST Noget af den enorme mængde spildte energi, som maskiner og enheder udsender som var
En lavtemperaturmetode til fremstilling af højtydende termoelektriske materialerMohamad Nugraha (til venstre) og hans gruppeleder, Derya Baran, demonstrere enhedens fleksibilitet. Kredit:KAUST Noget af den enorme mængde spildte energi, som maskiner og enheder udsender som var -
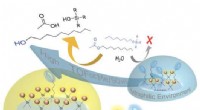 Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me -
 Forskere skaber fotoniske materialer til kraftfuld, effektiv lysbaseret databehandlingKredit:CC0 Public Domain Forskere fra University of Central Florida udvikler nye fotoniske materialer, der en dag kan hjælpe med at muliggøre laveffekt, ultrahurtig, lys-baseret databehandling. De
Forskere skaber fotoniske materialer til kraftfuld, effektiv lysbaseret databehandlingKredit:CC0 Public Domain Forskere fra University of Central Florida udvikler nye fotoniske materialer, der en dag kan hjælpe med at muliggøre laveffekt, ultrahurtig, lys-baseret databehandling. De


