Magnesium- og saltsyrereaktion:En detaljeret forklaring
* Reaktion: Magnesium (Mg) er et meget reaktivt metal. Når det kommer i kontakt med saltsyre, gennemgår det en enkelt fortrængningsreaktion. Hydrogenionerne (H+) i syren fortrænger magnesium fra dets metalliske form og danner magnesiumchlorid (MgCl2) og frigiver brintgas (H2).
Den kemiske ligning for denne reaktion er:
Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g)
* Observationer: Du vil bemærke flere ting under denne reaktion:
* Bobler: Frigivelsen af brintgas vil forårsage kraftig bobling.
* Varme: Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og opløsningen bliver mærkbart varm.
* Opløsning: Magnesiummetallet vil gradvist opløses, efterhånden som det reagerer med syren.
* Farveændring: Afhængigt af koncentrationen af syren kan opløsningen blive uklar eller ændre farve på grund af dannelsen af magnesiumchlorid.
Vigtige overvejelser:
* Sikkerhed: Denne reaktion er ret kraftig og producerer brændbar brintgas. Det bør kun udføres under strenge sikkerhedsforanstaltninger og med passende beskyttelsesudstyr.
* Korrosion: Saltsyre er ætsende, og reaktionen vil også korrodere alle metalbeholdere eller udstyr, der bruges i processen.
Opsummering: Reaktionen mellem saltsyre og magnesium er et klassisk eksempel på et metal, der reagerer med en syre og producerer salt, brintgas og varme.
 Varme artikler
Varme artikler
-
 Kemiens Alexa:Forskere på hurtig vej til at bygge åbent netværkKredit:CC0 Public Domain D. Tyler McQuade, Ph.D., professor ved Virginia Commonwealth University College of Engineering, er hovedefterforsker af et multi-universitetsprojekt, der søger at bruge ku
Kemiens Alexa:Forskere på hurtig vej til at bygge åbent netværkKredit:CC0 Public Domain D. Tyler McQuade, Ph.D., professor ved Virginia Commonwealth University College of Engineering, er hovedefterforsker af et multi-universitetsprojekt, der søger at bruge ku -
 Comet inspirerer til kemi til fremstilling af åndbar ilt på MarsKonstantinos P. Giapis med sin reaktor, der omdanner kuldioxid til molekylær oxygen. Kredit:California Institute of Technology Science fiction-historier er fyldt med terraforming-skemaer og iltgen
Comet inspirerer til kemi til fremstilling af åndbar ilt på MarsKonstantinos P. Giapis med sin reaktor, der omdanner kuldioxid til molekylær oxygen. Kredit:California Institute of Technology Science fiction-historier er fyldt med terraforming-skemaer og iltgen -
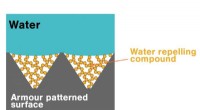 Super vandafvisende materialer er nu holdbare nok til den virkelige verdenEn skematisk fremstilling af, hvordan overfladen ser ud, og hvordan strukturen afviser vand. Kredit:Aalto Universitet Superhydrofobe overflader afviser vand som intet andet. Dette gør dem yderst a
Super vandafvisende materialer er nu holdbare nok til den virkelige verdenEn skematisk fremstilling af, hvordan overfladen ser ud, og hvordan strukturen afviser vand. Kredit:Aalto Universitet Superhydrofobe overflader afviser vand som intet andet. Dette gør dem yderst a -
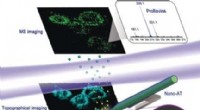 Kemisk og topografisk enkeltcelle-billeddannelse ved opløsning i nanoskala ved nærfeltsdesorptions…Kredit:Wiley Hvordan er kemikalier fordelt i en celle? Kinesiske videnskabsmænd har udviklet en kombineret massespektrometri og biologisk billeddannelsesenhed, der muliggør direkte, mærkefri påvis
Kemisk og topografisk enkeltcelle-billeddannelse ved opløsning i nanoskala ved nærfeltsdesorptions…Kredit:Wiley Hvordan er kemikalier fordelt i en celle? Kinesiske videnskabsmænd har udviklet en kombineret massespektrometri og biologisk billeddannelsesenhed, der muliggør direkte, mærkefri påvis
- Hvor mange lysår ville det tage at komme fra den ene ende af Mælkevejen anden?
- Hvor lang tid tager det solen at flytte en grad over under horisonten?
- Hvad starter en bølge-cut-platform med?
- Det henviser til energi i bevægelse?
- Giv ikke bjørnene mad! Sådan får parker besøgende til at beskytte naturen
- Hvad giver proteiner til cellen?


