Ioniske forbindelser:Hvordan modsat ladede ioner binder
Her er en oversigt:
* ioner: Atomer, der har fået eller mistet elektroner, hvilket resulterer i en netto positiv eller negativ ladning.
* Elektrostatiske kræfter: Tiltrækningskræfterne mellem modsatte ladninger.
Hvordan dannes ioniske forbindelser:
1. Overførsel af elektroner: Metaller (har tendens til at miste elektroner) reagerer med ikke-metaller (har tendens til at få elektroner). Metalatomet mister elektroner og bliver til en positivt ladet kation, mens ikke-metalatomet får elektroner og bliver en negativt ladet anion.
2. Attraktion: De modsat ladede ioner tiltrækkes af hinanden på grund af elektrostatiske kræfter og danner en ionbinding.
3. Krystalgitter: Ionerne arrangerer sig selv i en gentagen, tredimensionel struktur kaldet et krystalgitter, hvilket maksimerer tiltrækningen mellem modsatte ladninger og minimerer frastødning mellem ens ladninger.
Eksempler på ioniske forbindelser:
* Natriumchlorid (NaCl): Natrium (Na) mister en elektron for at danne Na⁺, og chlor (Cl) får en elektron til at danne Cl⁻. De modsat ladede ioner tiltrækkes af hinanden og danner forbindelsen natriumchlorid.
* Calciumoxid (CaO): Calcium (Ca) mister to elektroner for at danne Ca²⁺, og oxygen (O) får to elektroner til at danne O²⁻. Ionerne danner en stærk ionbinding i calciumoxid.
Lad mig vide, hvis du har yderligere spørgsmål om ioniske forbindelser!
 Varme artikler
Varme artikler
-
 Sådan klæber du sensorer til huden uden klæbemiddelKredit:Binghamton University Forestil dig, hvis du kunne sætte noget på din hud uden at have brug for lim. En biosensor, et ur, en kommunikationsenhed, et modetilbehør – mulighederne er uendelige.
Sådan klæber du sensorer til huden uden klæbemiddelKredit:Binghamton University Forestil dig, hvis du kunne sætte noget på din hud uden at have brug for lim. En biosensor, et ur, en kommunikationsenhed, et modetilbehør – mulighederne er uendelige. -
 Forskning giver potentielt bioblendstock til dieselbrændstofDerek Vardon og Nabila Huq fremviser en beholder med højtydende etherdiesel bioblendstock fremstillet hos NREL. Kredit:Dennis Schroeder, NREL NREL-forskerne, sammen med kolleger på Yale University
Forskning giver potentielt bioblendstock til dieselbrændstofDerek Vardon og Nabila Huq fremviser en beholder med højtydende etherdiesel bioblendstock fremstillet hos NREL. Kredit:Dennis Schroeder, NREL NREL-forskerne, sammen med kolleger på Yale University -
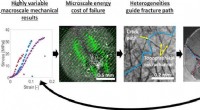
 Forskere udvikler genbrug til kulfiberkompositterWashington State University professor Jinwen Zhang med sit forskergruppe for genbrug af kulfiber. Kredit:Washington State University Et WSU -forskerhold har for første gang udviklet en lovende måd
Forskere udvikler genbrug til kulfiberkompositterWashington State University professor Jinwen Zhang med sit forskergruppe for genbrug af kulfiber. Kredit:Washington State University Et WSU -forskerhold har for første gang udviklet en lovende måd -
 Forskere afslører kritisk metabolisk switch for inflammatoriske sygdommeKredit:CC0 Public Domain Et forskerhold i Trinity College Dublin har afsløret en kritisk rolle for et protein kaldet PKM2 i reguleringen af immuncelletyper i hjertet af flere inflammatoriske syg
Forskere afslører kritisk metabolisk switch for inflammatoriske sygdommeKredit:CC0 Public Domain Et forskerhold i Trinity College Dublin har afsløret en kritisk rolle for et protein kaldet PKM2 i reguleringen af immuncelletyper i hjertet af flere inflammatoriske syg
- Enzym til biokatalyse bruger opløsningsmiddel som substrat
- Hvordan faktor X Squared Minus 2
- Hvor type energi afhænger af afstanden mellem to partikler og lades hver partikel?
- Hvilken rolle spiller mitokondrier?
- NEEMO:Test af rumudstyr under havet
- Hvad kommer til at tænke på, når du hører ordet energi?


