ClF5-hybridisering:en trin-for-trin guide til bestemmelse af central atomgeometri
1. Tegn Lewis-strukturen:
* Klor har 7 valenselektroner.
* Fluor har 7 valenselektroner.
* Der er 5 fluoratomer, så det er 5 * 7 =35 valenselektroner.
* Samlede valenselektroner:7 + 35 =42
* Placer kloratomet i midten.
* Omgiv den med 5 fluoratomer.
* Udfyld de resterende elektroner for at færdiggøre oktetter omkring fluoratomerne.
* Du vil opdage, at det centrale kloratom har 5 bindinger (til fluoratomerne) og et ensomt elektronpar.
2. Tæl det steriske nummer:
* Sterisk tal =antal atomer bundet til det centrale atom + antal enlige par på det centrale atom.
* I ClF5 er det steriske tal 5 + 1 =6.
3. Relater sterisk nummer til hybridisering:
* Sterisk tal på 6 svarer til sp³d² hybridisering .
Derfor er det centrale chloratom i ClF5 sp³d² hybridiseret.
Sidste artikelAtomer vs. Molecules:Forståelse af stoffets byggesten
Næste artikelLPG og biogas:Forståelse af fordelene ved renere brændstof
 Varme artikler
Varme artikler
-
 Akustisk mikrofluidisk platform adskiller forsigtigt og hurtigt cirkulerende tumorceller fra blodprø…Ved hjælp af lydbølger, et internationalt forskerteam har udviklet en blid, kontaktfri metode til adskillelse af cirkulerende tumorceller fra blodprøver, der er hurtig og effektiv nok til klinisk brug
Akustisk mikrofluidisk platform adskiller forsigtigt og hurtigt cirkulerende tumorceller fra blodprø…Ved hjælp af lydbølger, et internationalt forskerteam har udviklet en blid, kontaktfri metode til adskillelse af cirkulerende tumorceller fra blodprøver, der er hurtig og effektiv nok til klinisk brug -
 Direkte observation af kohærens energiskala af Hunds metalÆndring i den elektroniske struktur som følge af Se-doping x. I lavenergiregionen, der observeres et knæk - en brat ændring - i hældningen af båndstrukturen, og den bevæger sig til det lavere energi
Direkte observation af kohærens energiskala af Hunds metalÆndring i den elektroniske struktur som følge af Se-doping x. I lavenergiregionen, der observeres et knæk - en brat ændring - i hældningen af båndstrukturen, og den bevæger sig til det lavere energi -
 Nye glasmaterialer fremstillet af organiske og uorganiske komponenterDr. Courtney Calahoo fra University of Jena præsenterer organisk glas (l.) og uorganisk glas (r.) - to udgangsmaterialer til det nye kompositglas. Kredit:Jens Meyer/University of Jena Cambridge/Je
Nye glasmaterialer fremstillet af organiske og uorganiske komponenterDr. Courtney Calahoo fra University of Jena præsenterer organisk glas (l.) og uorganisk glas (r.) - to udgangsmaterialer til det nye kompositglas. Kredit:Jens Meyer/University of Jena Cambridge/Je -
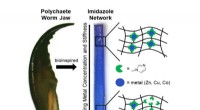 Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil
Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil


