Ioniske salte:Forståelse af dannelse og binding
* Elektronegativitet: Dette måler et atoms tendens til at tiltrække elektroner i en binding.
* Ionisk binding: Opstår, når det ene atom (det mere elektronegative) får elektroner og bliver til en anion (negativ ion), mens det andet atom mister elektroner og bliver til en kation (positiv ion). Den stærke elektrostatiske tiltrækning mellem disse modsat ladede ioner skaber ionbindingen.
Typiske eksempler:
* Metaller og ikke-metaller: Disse har normalt de mest signifikante elektronegativitetsforskelle. For eksempel er natrium (Na) et metal med lav elektronegativitet, og klor (Cl) er et ikke-metal med høj elektronegativitet. De reagerer og danner natriumchlorid (NaCl) eller bordsalt.
* Nogle ikke-metaller: Selv nogle ikke-metaller kan danne ioniske forbindelser med hinanden, hvis deres elektronegativitetsforskel er stor nok. Et godt eksempel er reaktionen mellem oxygen (O) og fluor (F) for at danne oxygendifluorid (OF2).
Nøgleudtag:
Dannelsen af et ionisk salt kræver, at det ene element er en stærk elektrondonor (metal eller et mindre elektronegativt ikke-metal), og det andet er en stærk elektronacceptor (ikke-metal eller et mere elektronegativt ikke-metal).
Sidste artikelKaliumchlorid ledningsevne:fast vs. smeltet tilstand forklaret
Næste artikelAt forstå atomet:Hvad fylder dets volumen?
 Varme artikler
Varme artikler
-
 Teknik kan hjælpe masseproduktion af bionedbrydeligt plastFibre af majsafledt, bionedbrydeligt plastik udviklet ved University of Nebraska-Lincoln. Nebraska-forskere og deres kolleger har demonstreret en ny teknik til forbedring af egenskaber ved bioplast, d
Teknik kan hjælpe masseproduktion af bionedbrydeligt plastFibre af majsafledt, bionedbrydeligt plastik udviklet ved University of Nebraska-Lincoln. Nebraska-forskere og deres kolleger har demonstreret en ny teknik til forbedring af egenskaber ved bioplast, d -
 Nyt energiomdannelseslag til biosolcellerEn bioelektrode med proteinkomplekset Fotosystem I under bestråling med rødt lys til måling af fotostrømmens respons. Kredit: Felipe Conzuelo Et forskerhold fra Ruhr-Universität Bochum (RUB), samm
Nyt energiomdannelseslag til biosolcellerEn bioelektrode med proteinkomplekset Fotosystem I under bestråling med rødt lys til måling af fotostrømmens respons. Kredit: Felipe Conzuelo Et forskerhold fra Ruhr-Universität Bochum (RUB), samm -
 Sammenligning af TEM og SEM:Hvordan transmissions- og scanningselektronmikroskoper adskiller sigAf Harvey Sells, opdateret 24. marts 2022 Transmissionselektronmikroskopi (TEM) og scanningselektronmikroskopi (SEM) er kraftfulde værktøjer til at visualisere strukturer på nanometerskalaen. Selvom
Sammenligning af TEM og SEM:Hvordan transmissions- og scanningselektronmikroskoper adskiller sigAf Harvey Sells, opdateret 24. marts 2022 Transmissionselektronmikroskopi (TEM) og scanningselektronmikroskopi (SEM) er kraftfulde værktøjer til at visualisere strukturer på nanometerskalaen. Selvom -
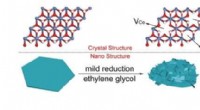 Rige defekter, der øger iltudviklingsreaktionenIllustration af den solvotermiske reaktion af uberørte CoFe LDHer ved at bruge ethylenglycol. Kredit:©Science China Press Iltudviklingsreaktionen (OER) med træg reaktionskinetik og stort overpoten
Rige defekter, der øger iltudviklingsreaktionenIllustration af den solvotermiske reaktion af uberørte CoFe LDHer ved at bruge ethylenglycol. Kredit:©Science China Press Iltudviklingsreaktionen (OER) med træg reaktionskinetik og stort overpoten
- En enhed, der bruges til at sammenligne masse af et objekt en kendt masse?
- Hvad er fair game på åbent hav?
- Hvilken proces er ikke en måde, hvorpå celler opretholder homeostase?
- Hvordan er revner i klipper i rette vinkler på overfladen?
- Termisk energilagring:Materiale absorberer varme, når det smelter og frigiver det, når det størkn…
- Hvilken tektonisk plade bærer kun hav?


