Koboltoxidationstal:Forståelse af variable tilstande og fælles værdier
Her er hvorfor:
* Overgangsmetaller: Cobalt er et overgangsmetal, og disse grundstoffer er kendt for at have variable oxidationstilstande.
* Elektronkonfiguration: Kobolts elektronkonfiguration gør det muligt for den at miste elektroner på forskellige måder, hvilket resulterer i forskellige positive ladninger (oxidationstilstande).
Almindelige oxidationstilstande for kobolt:
* +2: Dette er den mest almindelige oxidationstilstand, der findes i forbindelser som cobalt(II)chlorid (CoCl2) og cobalt(II)sulfat (CoSO4).
* +3: Denne oxidationstilstand er mindre almindelig, men stadig signifikant, set i forbindelser som cobalt(III)oxid (Co₂O3) og cobalt(III)chlorid (CoCl₃).
* Andre oxidationsstater: Cobalt kan også eksistere i oxidationstilstande på +1, +4 og endnu højere, men disse er sjældnere.
Bestemmelse af oxidationstilstand:
For at bestemme oxidationstilstanden for cobalt i en specifik forbindelse, skal du overveje ladningerne af de andre tilstedeværende grundstoffer og anvende reglen om, at summen af oxidationstilstande i en neutral forbindelse skal være lig med nul.
Eksempel:
I cobalt(II)oxid (CoO) har oxygen en oxidationstilstand på -2. Da forbindelsen er neutral, skal oxidationstilstanden for kobolt være +2 for at balancere ladningen.
 Varme artikler
Varme artikler
-
 Plane og buede pyrrol-fusionerede azacoronerπ-Udvidet azacoronen med en Janus dobbeltkonkav struktur Credit:Graduate School of Science and Engineering, Ehime Universitet Nylige undersøgelser af syntetiske tilgange til polycykliske aromatisk
Plane og buede pyrrol-fusionerede azacoronerπ-Udvidet azacoronen med en Janus dobbeltkonkav struktur Credit:Graduate School of Science and Engineering, Ehime Universitet Nylige undersøgelser af syntetiske tilgange til polycykliske aromatisk -
 Er det hamp eller marihuana? Ny scanner giver øjeblikkeligt svarHovedforfatter Lee Sanchez scanner et hampblad for THC, demonstrerer en af de snesevis af scanninger, han skulle udføre for at perfektionere holdets metode. Kredit:Dmitry Kurouski Hamp er teknis
Er det hamp eller marihuana? Ny scanner giver øjeblikkeligt svarHovedforfatter Lee Sanchez scanner et hampblad for THC, demonstrerer en af de snesevis af scanninger, han skulle udføre for at perfektionere holdets metode. Kredit:Dmitry Kurouski Hamp er teknis -
 Nye automatiserede biologiske prøveanalysesystemer til at fremskynde sygdomsopdagelseIllustration af de anvendte matematiske transformationer, først på billedet af et skakbræt, derefter på mikrofluidiske multipoler. Kredit:Polytechnique Montréal og McGill University Professor Thom
Nye automatiserede biologiske prøveanalysesystemer til at fremskynde sygdomsopdagelseIllustration af de anvendte matematiske transformationer, først på billedet af et skakbræt, derefter på mikrofluidiske multipoler. Kredit:Polytechnique Montréal og McGill University Professor Thom -
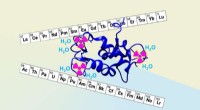 Gå ud over Moder Naturs molekyler for at målrette radioaktive metallerDet naturlige protein lanmodulin (afbildet i marineblåt) blev biokonstrueret af et samarbejde mellem forskere fra LLNL og Penn State University for bedre at opfange og adskille elementer fundet i nukl
Gå ud over Moder Naturs molekyler for at målrette radioaktive metallerDet naturlige protein lanmodulin (afbildet i marineblåt) blev biokonstrueret af et samarbejde mellem forskere fra LLNL og Penn State University for bedre at opfange og adskille elementer fundet i nukl
- Afstemning:Mindst en fjerdedel af asiatiske amerikanere rapporterer arbejdsplads, boligdiskriminatio…
- Hvilket af følgende er et målmaterialer evne til at transmittere væsker gennem sammenkoblede pore…
- Hvad er navnet, der gives til effekten af fældningsenergi i atmosfæren?
- Hvorfor kan genstande bevæge sig gennem væsker, men ikke faste stoffer?
- Eksport af naturgas:Langsom gang eller "farezone"?
- Hvad er en faktor ikke et stærkt bevis for evolution?


