Salpetersyre og bariumkarbonatreaktion:ligning og forklaring
2 HNO3 (vandigt) + BaCO3 (s) → Ba(NO3)2 (vandigt) + CO2 (g) + H2O (l)
Her er en oversigt over reaktionen:
* Reaktanter:
* Salpetersyre (HNO₃): En stærk syre.
* Bariumcarbonat (BaCO₃): Et hvidt fast stof.
* Produkter:
* Bariumnitrat (Ba(NO₃)₂): Et opløseligt salt.
* Culdioxid (CO₂): En farveløs gas.
* Vand (H₂O): En væske.
Forklaring:
Reaktionen forløber, fordi salpetersyre er en stærk syre og let donerer protoner (H⁺) til carbonationen (CO₃²⁻) fra bariumcarbonat. Denne protonering af karbonationen resulterer i dannelsen af kulsyre (H2CO3), som er ustabil og hurtigt nedbrydes til kuldioxid og vand.
Observationer:
* Du vil observere opbrusning (bobler), når der frigives kuldioxid.
* Opløsningen ville blive klar, når bariumcarbonatet opløses.
Sig til, hvis du har andre kemiske reaktioner, du gerne vil have hjælp til!
Sidste artikelFrancium Ion Formel:Forstå Fr⁺
Næste artikelBrint vs. vand:iltindhold forklaret - grundlæggende kemi
 Varme artikler
Varme artikler
-
 En allieret til legeringer:AI hjælper med at designe højtydende stålPNNLs særlige egenskaber ved at forbinde stål til aluminiumlegeringer muliggør lette køretøjsteknologier til bæredygtig transport. Kredit:Andrea Starr | Pacific Northwest National Laboratory Maski
En allieret til legeringer:AI hjælper med at designe højtydende stålPNNLs særlige egenskaber ved at forbinde stål til aluminiumlegeringer muliggør lette køretøjsteknologier til bæredygtig transport. Kredit:Andrea Starr | Pacific Northwest National Laboratory Maski -
 Materialer kan føre til selvhelbredende smartphonesEt nyt materiale helbreder ikke kun sig selv, men den strækker sig også op til 50 gange sin sædvanlige størrelse; disse egenskaber kan reparere din telefons batteri, hvis det revner, eller forhindre d
Materialer kan føre til selvhelbredende smartphonesEt nyt materiale helbreder ikke kun sig selv, men den strækker sig også op til 50 gange sin sædvanlige størrelse; disse egenskaber kan reparere din telefons batteri, hvis det revner, eller forhindre d -
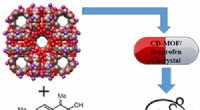 Længerevarende smertelindring med MOF'erKredit:American Chemical Society Til behandling af hovedpine, rygsmerter eller feber, de fleste af os har nået ibuprofen på et eller andet tidspunkt. Men vi skal ofte tage doser hver fjerde til sj
Længerevarende smertelindring med MOF'erKredit:American Chemical Society Til behandling af hovedpine, rygsmerter eller feber, de fleste af os har nået ibuprofen på et eller andet tidspunkt. Men vi skal ofte tage doser hver fjerde til sj -
 Turboladning af brændselsceller med en multifunktionel katalysatorEt nyt boost til brændselscelleteknologi fra Georgia Tech:En nanopartikelbelægning på denne disk turbolader forarbejdning af ilt på katodeenden af faste oxidbrændselsceller, øger den otte gange nuvæ
Turboladning af brændselsceller med en multifunktionel katalysatorEt nyt boost til brændselscelleteknologi fra Georgia Tech:En nanopartikelbelægning på denne disk turbolader forarbejdning af ilt på katodeenden af faste oxidbrændselsceller, øger den otte gange nuvæ
- Hvad er mængden af energi i en elektrisk ladning?
- Forskere skubber og trækker dråber med grafen
- Ny kvantemetode genererer virkelig tilfældige tal
- Konstellation der ligner en m?
- Undersøgelse forklarer, hvorfor jord og sand bliver stærkere, når de bliver ramt hårdere
- Forskning udforsker at fremme offentlig tillid til kunstig intelligens


