Beregning af nitrogenprocentsammensætning i (NH₄)₂HPO₄:en trin-for-trin guide
1. Bestem den molære masse af forbindelsen:
* N:14,01 g/mol (x 2) =28,02 g/mol
* H:1,01 g/mol (x 9) =9,09 g/mol
* P:30,97 g/mol
* O:16,00 g/mol (x 4) =64,00 g/mol
Total molær masse af (NH₄)₂HPO₄ =28,02 + 9,09 + 30,97 + 64,00 =132,08 g/mol
2. Beregn massen af nitrogen i et mol af forbindelsen:
* Masse af nitrogen =28,02 g/mol
3. Beregn den procentvise sammensætning af nitrogen:
* Procent sammensætning af nitrogen =(masse af nitrogen / molær masse af forbindelse) x 100%
* Procentsammensætning af nitrogen =(28,02 g/mol / 132,08 g/mol) x 100 %
* Procentsammensætning af nitrogen ≈ 21,22 %
Derfor er den procentvise sammensætning af nitrogen i (NH₄)₂HPO4 ca. 21,22 %.
Sidste artikelPoloniumoxidformel (PoO₂):Egenskaber og dannelse
Næste artikelOxygens bindingskapacitet:Forstå enkeltbindinger
 Varme artikler
Varme artikler
-
 Elektro-sprayede mikrodråber hjælper med at dræbe bakterier og viraFigur 1. Polymer mikrodysearray. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Med COVID-19 raser rundt om i verden, forskere fordobler metoder til at udvikle forskellige antim
Elektro-sprayede mikrodråber hjælper med at dræbe bakterier og viraFigur 1. Polymer mikrodysearray. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Med COVID-19 raser rundt om i verden, forskere fordobler metoder til at udvikle forskellige antim -
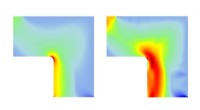 Materialegradienter kunne styrke polymerkomponenterGengivelser af, hvordan belastningen er fordelt på tværs af et L-formet beslag, der udelukkende er lavet af en stiv polymer (venstre) vs. et beslag med både stive og fleksible polymerer (højre). Kredi
Materialegradienter kunne styrke polymerkomponenterGengivelser af, hvordan belastningen er fordelt på tværs af et L-formet beslag, der udelukkende er lavet af en stiv polymer (venstre) vs. et beslag med både stive og fleksible polymerer (højre). Kredi -
 Flydende krystalmonomerer, der anvendes i LCD-skærme, der er fundet at være potentielt persistente…Kredit:CC0 Public Domain Et team af forskere fra Kina og Canada har fundet ud af, at flydende krystalmonomerer (LCMer), der bruges i LCDer, potentielt kan være persistente og bioakkumulerende. I d
Flydende krystalmonomerer, der anvendes i LCD-skærme, der er fundet at være potentielt persistente…Kredit:CC0 Public Domain Et team af forskere fra Kina og Canada har fundet ud af, at flydende krystalmonomerer (LCMer), der bruges i LCDer, potentielt kan være persistente og bioakkumulerende. I d -
 Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til
Ny tilgang forbedrer evnen til at forudsige metals reaktioner med vandVanddråbe. Billede:Wikimedia Commons Den brede rækkevidde af korrosion, et globalt problem på flere milliarder dollars, kan en dag blive indsnævret betydeligt takket være en ny, bedre tilgang til


