Forståelse af forbindelsers kogepunkter og flygtighed
Her er hvorfor:
* Intermolekylære kræfter: Flygtige forbindelser har svagere intermolekylære kræfter (som Van der Waals-kræfter) sammenlignet med ikke-flygtige forbindelser. Disse kræfter er ansvarlige for at holde molekyler sammen i en flydende tilstand. Svagere kræfter betyder, at der kræves mindre energi for at overvinde dem og bryde molekylerne fra hinanden, hvilket fører til lavere kogepunkter.
* Molekylvægt: Flygtige forbindelser har ofte lavere molekylvægte. Mindre molekyler har svagere intermolekylære kræfter, hvilket igen fører til lavere kogepunkter.
Eksempler på flygtige forbindelser og deres kogepunkter:
* Diethylether: Kogepunkt:34,6 °C
* Acetone: Kogepunkt:56,05 °C
* Methanol: Kogepunkt:64,7 °C
* Ethanol: Kogepunkt:78,37 °C
Det er vigtigt at bemærke, at:
* Kogepunktet for en forbindelse afhænger af forskellige faktorer, herunder tryk, og udtrykket "flygtig" er i forhold til den specifikke anvendelse og kontekst.
* Nogle forbindelser kan være flygtige ved stuetemperatur, men har stadig relativt høje kogepunkter. For eksempel har hexan et kogepunkt på 69 °C, men det anses stadig for flygtigt på grund af dets høje damptryk ved stuetemperatur.
Så i stedet for at tale om kogepunkter for flygtige forbindelser, er det mere præcist at sige, at flygtige forbindelser har en tendens til let at fordampe ved stuetemperatur på grund af deres svagere intermolekylære kræfter og lavere molekylvægte.
 Varme artikler
Varme artikler
-
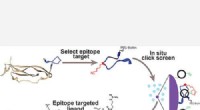 Bærbare sensorer kunne udnytte bioteknologi til at overvåge personlige, miljødataHurtig udviklingsproces af billig, meget stabile og modulære peptidbaserede syntetiske affinitetsmidler (PCCer) til proteinmål gennem brug af store peptidbiblioteker. Kredit:Genoptrykt med tilladelse
Bærbare sensorer kunne udnytte bioteknologi til at overvåge personlige, miljødataHurtig udviklingsproces af billig, meget stabile og modulære peptidbaserede syntetiske affinitetsmidler (PCCer) til proteinmål gennem brug af store peptidbiblioteker. Kredit:Genoptrykt med tilladelse -
 Et kemisk fingerpeg om, hvordan livet startede på JordenKredit:Scripps Institute Jorden rummer ikke altid liv. Men for omkring 4 milliarder år siden, noget i miljøet ændrede sig, og systemer med biologiske egenskaber begyndte at dukke op. Mange forsker
Et kemisk fingerpeg om, hvordan livet startede på JordenKredit:Scripps Institute Jorden rummer ikke altid liv. Men for omkring 4 milliarder år siden, noget i miljøet ændrede sig, og systemer med biologiske egenskaber begyndte at dukke op. Mange forsker -
 Svampeenzymer kan holde hemmeligheden bag fremstillingen af vedvarende energi fra træEn overordnet tredimensionel struktur af en af denne klasse af enzymer. Kredit:Professor Gideon Davies, University of York Et internationalt team af forskere, inklusive videnskabsmænd fra Univer
Svampeenzymer kan holde hemmeligheden bag fremstillingen af vedvarende energi fra træEn overordnet tredimensionel struktur af en af denne klasse af enzymer. Kredit:Professor Gideon Davies, University of York Et internationalt team af forskere, inklusive videnskabsmænd fra Univer -
 Det, vi vidste om vand, var trods alt rigtigtDannelsen af hydrogenperoxid ved luft-vand-grænsefladen i mikrodråber er ikke spontan som tidligere antaget, men er i stedet drevet af ozon. Kredit:KAUST En omfattende undersøgelse foretaget af K
Det, vi vidste om vand, var trods alt rigtigtDannelsen af hydrogenperoxid ved luft-vand-grænsefladen i mikrodråber er ikke spontan som tidligere antaget, men er i stedet drevet af ozon. Kredit:KAUST En omfattende undersøgelse foretaget af K
- Hvad er den producerede gas, når natrium reagerer med vand?
- Hvis et blad er fossiliseret, ville det sandsynligvis danne, hvilken type fossil?
- Hvordan kultur former biologi:Forståelse af samspillet
- Hvordan bevæger stoffer sig gennem cellemembranen?
- Hvor gode er tests for E. coli i vandløb?
- Deep learning neuralt netværk bruges til at detektere jordskælv


