Fluorgas påkrævet til ethylenkonvertering:En trinvis beregning
1. Afbalanceret kemisk ligning:
Reaktionen, du beskriver, er fluoreringen af ethylen (C₂H₄) for at producere 1,2-difluorethan (C₂H₄F₂):
C2H4 + 2F2 → C2H4F2
2. Moleberegninger:
* Moler C₂H₄F₂:
- Beregn molmassen af C₂H₄F₂:(2 * 12,01 g/mol) + (4 * 1,01 g/mol) + (2 * 19,00 g/mol) =66,06 g/mol
- Mol C₂H₄F₂ =(100 g) / (66,06 g/mol) =1,51 mol
* Moler F₂:
- Fra den afbalancerede ligning kræves der 2 mol F₂ for hver 1 mol C₂H₄F₂.
- Mol F2 =(1,51 mol C2H4F2) * (2 mol F2 / 1 mol C2H4F2) =3,02 mol F2
3. Volumenberegning:
* Ideel gaslov:
- Antag standard temperatur og tryk (STP):0 °C (273,15 K) og 1 atm.
- Ideel gaslov:PV =nRT, hvor:
- P =tryk (atm)
- V =volumen (L)
- n =mol
- R =ideel gaskonstant (0,0821 L·atm/mol·K)
- T =temperatur (K)
* Løsning for volumen:
- V =(nRT) / P
- V =(3,02 mol * 0,0821 L·atm/mol·K * 273,15 K) / 1 atm
- V ≈ 67,5 L
Derfor kræves ca. 67,5 liter fluorgas (F₂) for at omdanne 100 gram C₂H4 til C₂H₄F₂ ved STP.
Vigtig bemærkning: Fluorgas er ekstremt reaktiv og farlig. Denne beregning er kun til teoretisk forståelse og bør ikke forsøges i et laboratoriemiljø uden passende sikkerhedsforanstaltninger og ekspertise.
 Varme artikler
Varme artikler
-
 Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a
Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a -
 Ingeniører finder ud af, hvorfor nedfaldne blade på togskinner er så glatteKredit:Pixabay/CC0 Public Domain Et team af ingeniører ved University of Sheffield har fundet en forklaring på den ekstreme glathed på togskinner, når der er faldet løv på dem. I deres papir udgiv
Ingeniører finder ud af, hvorfor nedfaldne blade på togskinner er så glatteKredit:Pixabay/CC0 Public Domain Et team af ingeniører ved University of Sheffield har fundet en forklaring på den ekstreme glathed på togskinner, når der er faldet løv på dem. I deres papir udgiv -
 Kapsler i mikrostørrelse til målrettet lægemiddellevering inspireret af russisk pelmeniKredit:Pixabay/CC0 Public Domain Et internationalt team ledet af en Skoltech-forsker har udviklet en metode til fremstilling af bionedbrydelige polymermikrokapsler, gjort mere effektiv ved at henv
Kapsler i mikrostørrelse til målrettet lægemiddellevering inspireret af russisk pelmeniKredit:Pixabay/CC0 Public Domain Et internationalt team ledet af en Skoltech-forsker har udviklet en metode til fremstilling af bionedbrydelige polymermikrokapsler, gjort mere effektiv ved at henv -
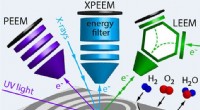 Tre mikroskoper ser mere end toGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.2c03692 Man skal se meget nøje for at forstå, hvilke processer der finder sted på overfladerne af katalysatorer. Faste katalysato
Tre mikroskoper ser mere end toGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.2c03692 Man skal se meget nøje for at forstå, hvilke processer der finder sted på overfladerne af katalysatorer. Faste katalysato
- Er brint den næst mest rigelige gas?
- Forståelse af opløselige organiske forbindelser og opløsninger
- Forskning undersøger årsagerne til fald i havniveauet i Det Døde Hav
- Et nyt biobrændstofsystem til brintproduktion fra biomasse
- Hvad hedder forbindelsen dannet med natrium og oxygenklor?
- Hvilken får jordtopografi til at ændre sig?


