Natriumchloriddannelse:Forståelse af ionisk binding og bordsalt (NaCl)
1. Natrium (Na) har 1 valenselektron i sin yderste skal, hvilket gør den meget reaktiv. Den ønsker at miste denne elektron for at opnå en stabil elektronkonfiguration som dens nærmeste ædelgas (Neon).
2. Klor (Cl) har 7 valenselektroner i dens yderste skal. Den har brug for en elektron mere for at opnå en stabil elektronkonfiguration som dens nærmeste ædelgas (Argon).
3. Elektronoverførsel: Natriumatomet afgiver let sin valenselektron til chloratomet. Denne overførsel resulterer i en positivt ladet natriumion (Na+) og en negativt ladet chloridion (Cl-).
4. Elektrostatisk tiltrækning: På grund af deres modsatte ladninger tiltrækkes natriumion og chloridion til hinanden. Denne elektrostatiske tiltrækning danner en ionisk binding , holder dem sammen som et molekyle af natriumchlorid (NaCl).
Vigtige takeaways:
* Ionbinding: Denne type binding opstår, når et metal (som natrium) mister en elektron til et ikke-metal (som klor).
* Stabil konfiguration: Både natrium og klor opnår en stabil elektronkonfiguration efter elektronoverførslen, hvilket gør forbindelsen mere stabil end de enkelte atomer.
* Ingen deling af elektroner: I modsætning til kovalente bindinger, i ionbindinger, overføres elektroner fuldstændigt, ikke delt.
Denne udveksling af elektroner er en grundlæggende proces i kemien, der fører til dannelsen af mange vigtige forbindelser.
 Varme artikler
Varme artikler
-
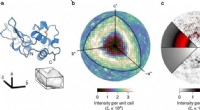 Forskere kortlægger proteinbevægelseret bånddiagram over lysozym (øverst) og den trikliniske enhedscelle, der indeholder et protein (nederst). b Der blev opnået et meget detaljeret tredimensionelt kort over diffus spredning. Den ydre kug
Forskere kortlægger proteinbevægelseret bånddiagram over lysozym (øverst) og den trikliniske enhedscelle, der indeholder et protein (nederst). b Der blev opnået et meget detaljeret tredimensionelt kort over diffus spredning. Den ydre kug -
 Forskere giver indsigt i letvægtsmateriale, der udvider sig med varmeKredit:Chong Min Koos gruppe ved Korea Institute of Science and Technology (KIST) Når det kommer til at tage plads uden at lægge for meget vægt, boblen kan ikke slås. Fordi de for det meste er luf
Forskere giver indsigt i letvægtsmateriale, der udvider sig med varmeKredit:Chong Min Koos gruppe ved Korea Institute of Science and Technology (KIST) Når det kommer til at tage plads uden at lægge for meget vægt, boblen kan ikke slås. Fordi de for det meste er luf -
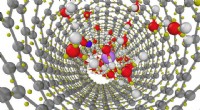 Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi
Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi -
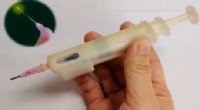 Handy pen lyser, når den udsættes for nervegas eller fordærvede maddampeDen praktiske pens spids skifter farve, når den udsættes for skadelige gasser. Kredit:Tilpasset fra ACS Materials Letters 2021, DOI:10.1021/acsmaterialslett.0c00516 Udsættelse for nogle lugtfri,
Handy pen lyser, når den udsættes for nervegas eller fordærvede maddampeDen praktiske pens spids skifter farve, når den udsættes for skadelige gasser. Kredit:Tilpasset fra ACS Materials Letters 2021, DOI:10.1021/acsmaterialslett.0c00516 Udsættelse for nogle lugtfri,
- Hvad er forskellen mellem en menneskelig livscyklus til Stars Life?
- Fotosyntese:Hvordan planter bruger sollys til energi og vækst
- Vandsektorvirksomheder:hvilke vil synke eller svømme?
- Bruger atomkraftværker uran til at producere energi?
- Hvad er de fire metoder til at adskille en mekanisk blanding?
- Hvordan producerer forbrændingen af biomasse energi?


