Forståelse af svovlsyres styrke:fuldstændig ionisering forklaret
1. Fuldstændig ionisering:
* Når svovlsyre opløses i vand, donerer den let begge sine hydrogenioner (H+) til vandmolekyler og danner hydroniumioner (H₃O+). Denne proces er i det væsentlige irreversibel, hvilket betyder, at den fortsætter næsten helt til fuldførelse.
* Reaktionen kan repræsenteres som:
H2S04 (vandig) + 2H2O (l) → 2H3O+ (vandig) + SO42- (vandig)
2. Høj ioniseringskonstant (Ka):
* Ioniseringskonstanten (Ka) er et mål for en syres styrke. En højere Ka-værdi indikerer en stærkere syre.
* Svovlsyre har en meget høj Ka-værdi, hvilket indikerer, at den let donerer protoner (H+) og danner en stor mængde hydroniumioner.
3. Stærk elektrolyt:
* På grund af dens fuldstændige ionisering betragtes svovlsyre som en stærk elektrolyt. Det betyder, at den leder elektricitet meget godt i opløsning.
4. Reaktivitet:
* Svovlsyrens stærke surhed afspejles i dens høje reaktivitet. Det reagerer let med mange stoffer, herunder metaller, baser og endda vand selv, og genererer varme i processen.
Opsummering:
Kombinationen af fuldstændig ionisering, høj ioniseringskonstant og høj reaktivitet gør svovlsyre til en stærk syre. Dens evne til let at donere begge sine hydrogenioner og danne en stor koncentration af hydroniumioner i opløsning er den definerende egenskab ved dens styrke.
Sidste artikelIonisk ladning:Forståelse af positive ladninger i atomer
Næste artikelKulstof:Egenskaber og klassificering som ikke-metal
 Varme artikler
Varme artikler
-
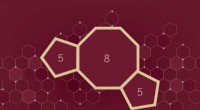 Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm
Gennembrudssyntesestrategi kan betyde bølge af nye medicinske forbindelserFSU-forskere har udtænkt en strategi til syntetisering af carbocykliske 5-8-5 smeltede ringsystemer, en molekylær struktur med potentielt bredt terapeutisk potentiale. Kredit:Benjamin Moten I farm -
 Forskere finder en ny metode til at kontrollere elektroniske egenskaber af nanokrystallerFra venstre mod højre:XPD-strålelinjeforsker Sanjit Ghose, postdoktor Anna Plonka, og Brookhaven kemiker Anatoly Frenkel. Kredit:Brookhaven National Laboratory Forskere fra The Hebrew University o
Forskere finder en ny metode til at kontrollere elektroniske egenskaber af nanokrystallerFra venstre mod højre:XPD-strålelinjeforsker Sanjit Ghose, postdoktor Anna Plonka, og Brookhaven kemiker Anatoly Frenkel. Kredit:Brookhaven National Laboratory Forskere fra The Hebrew University o -
 Almindelige husholdningsbaser og syrer:anvendelser, egenskaber og sikkerhedstipAf Natasha Gilani Opdateret 24. marts 2022 JPC-PROD/iStock/GettyImages En kemisk base, eller alkalisk, accepterer hydrogenioner (H+ ) and typically dissolves in water to conduct electricity. Bases t
Almindelige husholdningsbaser og syrer:anvendelser, egenskaber og sikkerhedstipAf Natasha Gilani Opdateret 24. marts 2022 JPC-PROD/iStock/GettyImages En kemisk base, eller alkalisk, accepterer hydrogenioner (H+ ) and typically dissolves in water to conduct electricity. Bases t -
 Forskere rapporterer om en ny tilstand af stof beskrevet som flydende glasPlaceringen og orienteringen af ellipsoide partikler i klynger af et flydende glas. Kredit:Forskningsgrupper af professor Andreas Zumbusch og professor Matthias Fuchs Opdagelsen af flydende gl
Forskere rapporterer om en ny tilstand af stof beskrevet som flydende glasPlaceringen og orienteringen af ellipsoide partikler i klynger af et flydende glas. Kredit:Forskningsgrupper af professor Andreas Zumbusch og professor Matthias Fuchs Opdagelsen af flydende gl
- Magneter ødelægger disketter, hvad ødelægger det ellers?
- Et blødt robotinsekt, der overlever at blive fladtrykt af en fluesmatter
- Hvor meget energi har en person brug for i dag joules?
- Almindelig herbicidforbindelse kan redde millioner af liv
- Er tordenvejr i begge jordmåne?
- Hvad er overførslen af energi som varme gennem et stof ved direkte kontakt?


