Vandbindinger:Hydrogen vs. ionisk - Forståelse af molekylære interaktioner
Her er hvorfor:
* ioniske bindinger dannes mellem modsat ladede ioner (atomer, der har fået eller mistet elektroner). Vandmolekyler (H2O) er neutrale og danner ikke ioner.
* Brintbindinger dannes mellem et brintatom, der er kovalent bundet til et stærkt elektronegativt atom (som oxygen i vand) og et elektronpar i det tilstødende molekyle. Dette skaber en svag tiltrækning mellem molekylerne.
Hydrogenbindingerne i vand er ansvarlige for mange af dets unikke egenskaber, såsom dets høje kogepunkt, høje overfladespænding og evne til at opløse mange stoffer.
 Varme artikler
Varme artikler
-
 Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod
Nyt krystallinsk oxid kan løse problemet med overophedning i kompositmaterialerKredit:Toshihiro Isobe, Tokyo Institute of Technology Forskere ved Tokyo Institute of Technology har for nylig syntetiseret et nyt materiale, der viser unikke termiske ekspansionsegenskaber. Metod -
 At bryde reglerne:Tunge kemiske grundstoffer ændrer teorien om kvantemekanikThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/FSU Photography Services En række komplicerede eksperimenter, der involverer et af de m
At bryde reglerne:Tunge kemiske grundstoffer ændrer teorien om kvantemekanikThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/FSU Photography Services En række komplicerede eksperimenter, der involverer et af de m -
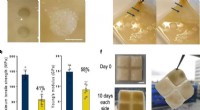 Selvhelbredende levende materialer brugt som 3D byggeklodserForskere så fremragende reparation, der var strukturelt stabil og genoprettede materialets konsistens og udseende. Kredit:Imperial College London Imperial College London-forskere har skabt 3D-bygg
Selvhelbredende levende materialer brugt som 3D byggeklodserForskere så fremragende reparation, der var strukturelt stabil og genoprettede materialets konsistens og udseende. Kredit:Imperial College London Imperial College London-forskere har skabt 3D-bygg -
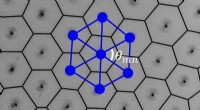 Forskere skaber aktivt materiale ud af mikroskopiske spindende partiklerSelvsamlet dynamisk gitter af spinnere. Voronoi-diagrammet er overlejret med det observerede gitter. Spinnerne er slørede på grund af den lange eksponeringstid, der muliggjorde præcis identifikation a
Forskere skaber aktivt materiale ud af mikroskopiske spindende partiklerSelvsamlet dynamisk gitter af spinnere. Voronoi-diagrammet er overlejret med det observerede gitter. Spinnerne er slørede på grund af den lange eksponeringstid, der muliggjorde præcis identifikation a
- Hvordan er kræfter relateret til bevægelse?
- Visualisering af debris disk roller derby for at forstå planetarisk systemudvikling
- Planter laver deres egen mad ved hjælp af energi, der kommer fra hvad?
- Første luminescerende molekylære system med en lavere kritisk opløsningstemperatur
- Kan koraller redde vores have? Forskere opdager, at blødt væv kan hjælpe med at beskytte rev
- Nem aluminium nanopartikler til hurtig, effektiv brintgenerering fra vand


