Natriumhydroxid vs. saltsyre:Forståelse af kemisk styrke
Her er hvorfor:
* Natriumhydroxid (NaOH) er en stærk base. Baser er stoffer, der kan acceptere brintioner (H+). Stærke baser dissocierer fuldstændigt i opløsning, hvilket betyder, at de frigiver alle deres hydroxidioner (OH-), hvilket gør opløsningen meget alkalisk.
* Saltsyre (HCl) er en stærk syre. Syrer er stoffer, der kan donere brintioner (H+). Stærke syrer dissocierer fuldstændigt i opløsning og frigiver alle deres hydrogenioner (H+), hvilket gør opløsningen meget sur.
Så i stedet for "stærkere" bør vi bruge udtryk, der nøjagtigt afspejler deres egenskaber:
* Natriumhydroxid er mere basisk end saltsyre.
* Saltsyre er surere end natriumhydroxid.
Tænk på det på denne måde:
* Syrer og baser er på et spektrum. De måles ved hjælp af en pH-skala, hvor 0 er det sureste og 14 er det mest basiske.
* Natriumhydroxid har en høj pH, hvilket gør det til en stærk base.
* Saltsyre har en lav pH, hvilket gør det til en stærk syre.
I sidste ende kan både natriumhydroxid og saltsyre være farlige, hvis de ikke håndteres korrekt. Begge er ætsende og kan forårsage alvorlige forbrændinger.
 Varme artikler
Varme artikler
-
 En ny, naturlig voksbelægning gør beklædningsgenstande vandtætte og åndbareKredit:Aalto University Der er en stigende bekymring over miljøpåvirkningen af tekstilproduktion, og mange vandtætte produkter på markedet er fremstillet med giftige kemikalier. Dette øger efter
En ny, naturlig voksbelægning gør beklædningsgenstande vandtætte og åndbareKredit:Aalto University Der er en stigende bekymring over miljøpåvirkningen af tekstilproduktion, og mange vandtætte produkter på markedet er fremstillet med giftige kemikalier. Dette øger efter -
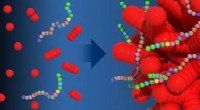 Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ -
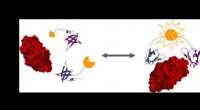 At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at
At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at -
 Belysning af hydrogeler via nanomaterialerDenne visuelle fremstilling demonstrerer, hvordan lys? Reagerende hydrogeler absorberer og konverterer nær-infrarødt lys til varme, som kan udvikles til at styre termoresponsive materialer. Kredit:Dr.
Belysning af hydrogeler via nanomaterialerDenne visuelle fremstilling demonstrerer, hvordan lys? Reagerende hydrogeler absorberer og konverterer nær-infrarødt lys til varme, som kan udvikles til at styre termoresponsive materialer. Kredit:Dr.
- Hvor Wecan ikke lysende krop gøres lysende krop?
- Iboende ustablet dobbeltlagsgrafen til højhastigheds lithium-svovl-batterier
- Laserstråler til superledning:Forskning kaster lys over uventede fysiske fænomener
- Hvad opstår, når Suns mest direkte stråler rammer ækvator- og dagoplevelser lige store mængder …
- Stiger luftfugtigheden, når temperaturen stiger?
- Hvad er forbundet med kinetisk energi af elektricitet?


