Calciummetal- og salpetersyrereaktion:Produkter, forklaring og sikkerhed
Reaktionsligning:
Ca(s) + 2HNO₃(aq) → Ca(NO3)₂) (aq) + H₂(g) + Heat
Forklaring:
1. Calcium (Ca) oxideres: Calciummetal mister elektroner og danner calciumioner (Ca²⁺).
2. Salpetersyre (HNO3) reduceres: Hydrogenionerne (H⁺) fra salpetersyre får elektroner til at danne brintgas (H₂).
3. Calciumnitrat (Ca(NO₃)₂) dannes: Calciumioner (Ca²⁺) reagerer med nitrationer (NO₃⁻) fra syren og danner calciumnitrat, et opløseligt salt.
4. Brintgas (H₂) frigives: Hydrogengas produceres som et biprodukt af reaktionen og frigives som bobler.
5. Varme frigives: Reaktionen er eksoterm, hvilket betyder, at den frigiver varme og gør opløsningen varm.
Yderligere bemærkninger:
* Sidereaktioner: Salpetersyre kan yderligere reagere med den producerede brintgas, hvilket også fører til dannelsen af nitrogenoxider (NOx). Dette er især sandsynligt, hvis koncentrationen af salpetersyre er høj.
* Sikkerhed: Reaktionen er meget eksoterm og kan være farlig, hvis den ikke håndteres med omhu. Bær altid passende sikkerhedsudstyr, såsom handsker og beskyttelsesbriller, og arbejd i et godt ventileret område.
Samlet set: Reaktionen mellem calcium og salpetersyre er et klassisk eksempel på en enkelt fortrængningsreaktion, hvor et mere reaktivt metal (calcium) fortrænger et mindre reaktivt grundstof (brint) fra sin forbindelse. Reaktionen resulterer i dannelse af calciumnitrat, brintgas og frigivelse af varme.
Sidste artikelNatriumchlorid:Forstå udtrykket 'salt'
Næste artikelDehydromenthofurolacton (DMFL):Kemiske egenskaber og struktur
 Varme artikler
Varme artikler
-
 Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon
Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon -
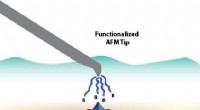 Virusoverflader hjælper ingeniører med at studere vaccine- og genterapiapplikationerEt isoelektrisk punkt er en almindelig måde at karakterisere vira på. Imidlertid, det er ikke nemt. For at forbedre fremstillingen af vacciner og genterapi, et Michigan Tech-team bruger overfladelad
Virusoverflader hjælper ingeniører med at studere vaccine- og genterapiapplikationerEt isoelektrisk punkt er en almindelig måde at karakterisere vira på. Imidlertid, det er ikke nemt. For at forbedre fremstillingen af vacciner og genterapi, et Michigan Tech-team bruger overfladelad -
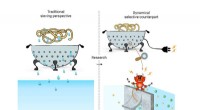 Aktiv sigtning kunne forbedre dialyse- og vandrensningsfiltreFor at adskille molekyler bruges normalt et colander-filter (venstre side). En ny type filter, hvor hullerne i sien kan aktiveres udforskes. (Højre side) Takket være en ekstern strømindgang, hullerne
Aktiv sigtning kunne forbedre dialyse- og vandrensningsfiltreFor at adskille molekyler bruges normalt et colander-filter (venstre side). En ny type filter, hvor hullerne i sien kan aktiveres udforskes. (Højre side) Takket være en ekstern strømindgang, hullerne -
 Leviathan polymer børste lavet med E. coli holder bakterier i skakMikroskopisk monster:Et tilfældigt øjeblik i laboratoriet førte til skabelsen af polymerbørster 100 gange den sædvanlige størrelse. Børsterne er synlige under mikroskopet, hvorimod polymerbørster no
Leviathan polymer børste lavet med E. coli holder bakterier i skakMikroskopisk monster:Et tilfældigt øjeblik i laboratoriet førte til skabelsen af polymerbørster 100 gange den sædvanlige størrelse. Børsterne er synlige under mikroskopet, hvorimod polymerbørster no


