Reaktion af zinksulfid med saltsyre:produkter og forklaring
* Hydrogensulfidgas (H₂S) er frigivet. Denne gas har en karakteristisk lugt af rådne æg.
* Zinkchloridopløsning (ZnCl₂) er dannet.
Den afbalancerede kemiske ligning for denne reaktion er:
ZnS(s) + 2HCl(aq) → ZnCl2(aq) + H2S(g)
Her er hvad der sker:
1. Saltsyre (HCl) er en stærk syre, hvilket betyder, at den let donerer protoner (H⁺-ioner) i opløsning.
2. Zinksulfid (ZnS) er et fast stof, der opløses i nærvær af syre.
3. H⁺-ionerne fra HCl reagerer med sulfidionerne (S²⁻) fra ZnS og danner hydrogensulfid (H2S) , en svag syre, der eksisterer som en gas ved stuetemperatur.
4. zinkionerne (Zn²⁺) fra ZnS kombineres med chloridionerne (Cl⁻) fra HCl for at danne zinkchlorid (ZnCl2) , som forbliver opløst i opløsningen.
Det er vigtigt at bemærke, at svovlbrintegas er meget giftig og skal håndteres med ekstrem forsigtighed i et godt ventileret område.
 Varme artikler
Varme artikler
-
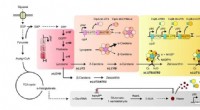 Metabolisk manipuleret bakterie producerer luteinSystemets metaboliske teknik blev anvendt til at konstruere og optimere de metaboliske veje til luteinproduktion, og substratkanalisering og elektronkanaliseringsstrategier blev desuden anvendt til at
Metabolisk manipuleret bakterie producerer luteinSystemets metaboliske teknik blev anvendt til at konstruere og optimere de metaboliske veje til luteinproduktion, og substratkanalisering og elektronkanaliseringsstrategier blev desuden anvendt til at -
 Stivelse vs glykogen:Hvordan planter og dyr opbevarer kulhydraterAf John Brennan Opdateret 24. marts 2022 Nednapa/iStock/GettyImages Når du tænker på stivelse, forestiller du dig sandsynligvis verdens basisfødevarer - majs, kartofler, ris. Stivelse er den primær
Stivelse vs glykogen:Hvordan planter og dyr opbevarer kulhydraterAf John Brennan Opdateret 24. marts 2022 Nednapa/iStock/GettyImages Når du tænker på stivelse, forestiller du dig sandsynligvis verdens basisfødevarer - majs, kartofler, ris. Stivelse er den primær -
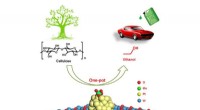 Forskere udvikler en kemokatalytisk tilgang til one-pot-reaktion af celluloseholdig ethanolOne-pot produktion af celluloseholdig ethanol via tandem katalyse over multifunktionel Mo/Pt/WOx katalysator Kredit:WANG Aiqin Forskere ved Dalian Institute of Chemical Physics (DICP) fra det kine
Forskere udvikler en kemokatalytisk tilgang til one-pot-reaktion af celluloseholdig ethanolOne-pot produktion af celluloseholdig ethanol via tandem katalyse over multifunktionel Mo/Pt/WOx katalysator Kredit:WANG Aiqin Forskere ved Dalian Institute of Chemical Physics (DICP) fra det kine -
 Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
- At studere Fraunhofer -linjer hjælper med at identificere, hvad der på stjernerne?
- Theres nu en bedre måde at beregne din pups alder i "menneskelige år"
- Hvilken type energi bruges til en vægstik?
- Hvilken proces får sandkorn til at danne en sandsten?
- Googles Art Transfer giver brugerne mulighed for at transformere billeder, som om de var malet af be…
- Hvordan beregner du antallet af nuetroner i et atom?


