Xenon-reaktivitet:Forståelse af ædelgasundtagelsen
Men xenon er ikke fuldstændig ureaktivt . Under visse forhold kan det danne forbindelser, specifikt med stærkt elektronegative elementer som fluor og oxygen. Disse forbindelser anses generelt for at være meget ustabile og kræver særlige betingelser for at danne.
Her er en oversigt over xenons reaktivitet:
* Normale forhold: Xenon er ekstremt ureaktivt og danner ikke let forbindelser.
* Ekstreme forhold:
* Højtryk og temperatur: Kan føre til dannelse af forbindelser som XeF2 , XeF4 og XeO3 .
* Tilstedeværelse af stærke oxidationsmidler: Disse kan reagere med xenon og danne forbindelser som XeO2 og XeO4 .
Eksempler på xenonforbindelser:
* Xenon-difluorid (XeF2 ): Et farveløst fast stof, der bruges i nogle laserapplikationer.
* Xenon-tetrafluorid (XeF4 ): Et hvidt fast stof, der anvendes til syntese af andre xenonforbindelser.
* Xenonhexafluorid (XeF6 ): En farveløs gas, der bruges som fluoreringsmiddel.
Samlet set, mens xenon betragtes som en ædelgas og generelt ikke er reaktiv, kan det danne forbindelser under specifikke forhold. Denne reaktivitet, selvom den er begrænset, har ført til interessante opdagelser og anvendelser på forskellige områder.
Sidste artikelJern- og iltreaktivitet:Forståelse af deres kemiske adfærd
Næste artikelKemiske reaktioners vitale rolle i livet
 Varme artikler
Varme artikler
-
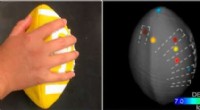 Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man
Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man -
 Pulserne stiger, da ny undersøgelse afslører plantens hemmeligheder, der holder folk i roBeroligende indflydelse -- Indisk Snakeroot. Kredit:John Innes Center Kemiske hemmeligheder for en plante, der er blevet brugt gennem historien for dens beroligende virkning, er blevet afsløret i
Pulserne stiger, da ny undersøgelse afslører plantens hemmeligheder, der holder folk i roBeroligende indflydelse -- Indisk Snakeroot. Kredit:John Innes Center Kemiske hemmeligheder for en plante, der er blevet brugt gennem historien for dens beroligende virkning, er blevet afsløret i -
 Aluminiumsulfat og hydreret kalk:Sådan renser de drikkevandVandbehandling er en sofistikeret proces, der er afhængig af en række kemikalier til at omdanne råt, ubehandlet vand til en sikker drikkevare af høj kvalitet. Ved at binde og fjerne urenheder, dræbe b
Aluminiumsulfat og hydreret kalk:Sådan renser de drikkevandVandbehandling er en sofistikeret proces, der er afhængig af en række kemikalier til at omdanne råt, ubehandlet vand til en sikker drikkevare af høj kvalitet. Ved at binde og fjerne urenheder, dræbe b -
 FBI retsmedicin rammer Hollywood fart, siger forskerKredit:Florida International University Hvis du tror på alt, hvad du ser på tv, retsmedicinere kan afslutte en sag på en time. Det sker ikke i det virkelige liv. Indtil det gør, sagde professor S
FBI retsmedicin rammer Hollywood fart, siger forskerKredit:Florida International University Hvis du tror på alt, hvad du ser på tv, retsmedicinere kan afslutte en sag på en time. Det sker ikke i det virkelige liv. Indtil det gør, sagde professor S


