Hydrogenbindinger i vand:Forståelse af samhørighed
Her er hvorfor:
* Brintbindinger er relativt svage bindinger, der dannes mellem et brintatom, der er kovalent bundet til et stærkt elektronegativt atom (som oxygen i vand) og et elektronpar i det tilstødende molekyle.
* I vand er iltatomet mere elektronegativt end hydrogenatomerne, hvilket skaber en delvis negativ ladning på ilten og en delvis positiv ladning på brinten.
* Disse delladninger tiltrækker modsatte ladninger på nabovandmolekyler og danner brintbindinger.
Disse hydrogenbindinger er ansvarlige for de stærke sammenhængskræfter mellem vandmolekyler, hvilket fører til egenskaber som:
* Høj overfladespænding: Sammenhængskræfterne gør det svært at bryde vandoverfladen.
* Højt kogepunkt: Hydrogenbindinger kræver betydelig energi for at bryde, hvilket fører til et højt kogepunkt for vand.
* Kapillærvirkning: Sammenhængskræfterne mellem vandmolekyler og klæbekræfterne mellem vand og væggene i smalle rør resulterer i kapillærvirkning.
Sammenfattende er hydrogenbindinger nøglen til vandets sammenhængende natur, hvilket bidrager til dets unikke egenskaber.
Sidste artikelK2CO3 kemisk formel:Forståelse af kaliumcarbonat
Næste artikelProteinhydrolyse:Produkter og fordele - En omfattende guide
 Varme artikler
Varme artikler
-
 Magnetiske bakterier som mikropumperKredit:Unsplash/CC0 Public Domain ETH-forskere bruger magnetiske bakterier til at kontrollere væsker på mikroniveau. De overvejer allerede at bruge dem i den menneskelige blodbane til præcis lever
Magnetiske bakterier som mikropumperKredit:Unsplash/CC0 Public Domain ETH-forskere bruger magnetiske bakterier til at kontrollere væsker på mikroniveau. De overvejer allerede at bruge dem i den menneskelige blodbane til præcis lever -
 Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender
Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender -
 Forskere ramte protein- og lipidsammensætningen af den sibiriske mammutknogleKredit:@tsarcyanide/MIPT Forskere fra Skoltech og Moskva Institut for Fysik og Teknologi (MIPT) undersøgte protein- og lipidsammensætningen af en mammutknogle fundet nær Yana -floden i det nordø
Forskere ramte protein- og lipidsammensætningen af den sibiriske mammutknogleKredit:@tsarcyanide/MIPT Forskere fra Skoltech og Moskva Institut for Fysik og Teknologi (MIPT) undersøgte protein- og lipidsammensætningen af en mammutknogle fundet nær Yana -floden i det nordø -
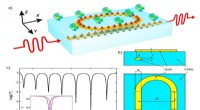 Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi
Blod og sved:Bærbare medicinske sensorer vil få et stort følsomhedsforøgelseBiosensor layout (en, c). Bølgelederen er inde i det dielektriske substrat. Resonatoren, realiseret som en ringbølgeleder, er placeret ved grænsefladen mellem det dielektriske materiale og den biologi
- Hvordan ændres bevægelsen af vandmolekyler under frysning?
- Hvilket organ kontrollerer alle andre kropssystemer?
- Hvor mange æg er 170 gram?
- Hvad er overførslen af energi som varme gennem et stof ved direkte kontakt?
- Hvordan relaterer hydroxid- og hydrogenioner til syrebaser?
- Waymo -chef siger, at hans teknologi ville have afværget et fatalt Uber -nedbrud


