Forståelse af formler for ioniske forbindelser:Hvorfor Lewis-teorien ikke er nok
Hvorfor kommer Lewis-teorien til kort:
* Elektronoverførsel, ikke deling: Ioniske forbindelser dannes ved fuldstændig overførsel af elektroner fra et metal (kationer) til et ikke-metal (anioner). Lewis-strukturer fokuserer på at dele elektroner, hvilket ikke nøjagtigt repræsenterer arten af ionbinding.
* Elektrostatisk attraktion: Den primære kraft, der holder ioniske forbindelser sammen, er den elektrostatiske tiltrækning mellem modsat ladede ioner. Lewis-strukturer skildrer ikke eksplicit denne attraktion.
* Gitterstruktur: Ioniske forbindelser eksisterer i et 3D-krystalgitter, ikke som individuelle molekyler som afbildet i Lewis-strukturer.
Sådan bestemmes formler for ionforbindelser:
1. Identificer ionerne: Bestem ladningerne for den involverede kation og anion. Dette gøres normalt ved at henvise til det periodiske system og kende almindelige polyatomiske ioner.
2. Balancer afgifterne: Formlen for en ionforbindelse skal være elektrisk neutral. Brug subscripts til at angive antallet af hver ion, der kræves for at opnå denne neutralitet.
3. Eksempel: Natrium (Na+) og chlorid (Cl-) danner natriumchlorid (NaCl). En natriumion med +1 ladning balancerer en chloridion med -1 ladning.
Opsummering: Mens Lewis teori er værdifuld for at forstå kovalente bindinger, er det ikke det rigtige værktøj til at bestemme formler for ionforbindelser. At forstå ionladninger og balancerende ladninger er afgørende for at forudsige sammensætningen af ioniske forbindelser.
Sidste artikelIlttank:Forstå masse vs. tryk – er halvt tom?
Næste artikelGilbert Lewis og Lewis Acid-Base Theory:Elektronpardonation
 Varme artikler
Varme artikler
-
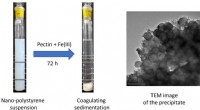 Interaktion mellem nanoplast og pektin, et vandopløseligt polysaccharidVenstre billede:Billedet af en nano-polystyrensuspension (500 mg L−1, pH 7) (venstre) og nanopolystyrensuspensionen efter tilsætning af pektin (15 mg L−1) og Fe(III) (0,10 mM) efter opbevaring i 72 ti
Interaktion mellem nanoplast og pektin, et vandopløseligt polysaccharidVenstre billede:Billedet af en nano-polystyrensuspension (500 mg L−1, pH 7) (venstre) og nanopolystyrensuspensionen efter tilsætning af pektin (15 mg L−1) og Fe(III) (0,10 mM) efter opbevaring i 72 ti -
 Meget stabil vandelektrolysekatalysator til produktion af brint og oxygenSkematisk diagram over foreslåede gebyroverførselsprocesser mellem MoSe 2 og LSC. Kredit:UNIST En nylig undersøgelse, tilknyttet UNIST har præsenteret ædle katalysatorer til vandelektrolyse, i s
Meget stabil vandelektrolysekatalysator til produktion af brint og oxygenSkematisk diagram over foreslåede gebyroverførselsprocesser mellem MoSe 2 og LSC. Kredit:UNIST En nylig undersøgelse, tilknyttet UNIST har præsenteret ædle katalysatorer til vandelektrolyse, i s -
 Trin-for-trin guide:Opbygning af en 3D-model af et beryllium-atomAf Michael E Carpenter Opdateret 24. marts 2022 Beryllium, eller Be, er atomnummer 4 i grundstoffernes periodiske system. Det betyder, at berylliumatomet har fire protoner og fire elektroner. Antal
Trin-for-trin guide:Opbygning af en 3D-model af et beryllium-atomAf Michael E Carpenter Opdateret 24. marts 2022 Beryllium, eller Be, er atomnummer 4 i grundstoffernes periodiske system. Det betyder, at berylliumatomet har fire protoner og fire elektroner. Antal -
 Forskere opdager en hurtigere måde at fremstille vaskulære materialer påSynkroniseret fremstilling af en bioinspireret struktur med et hierarkisk vaskulært netværk. Kredit:Mayank Garg, Nancy Sottos, Jeff Moore, og Phillipe Guebelle At udvikle selvhelbredende materiale
Forskere opdager en hurtigere måde at fremstille vaskulære materialer påSynkroniseret fremstilling af en bioinspireret struktur med et hierarkisk vaskulært netværk. Kredit:Mayank Garg, Nancy Sottos, Jeff Moore, og Phillipe Guebelle At udvikle selvhelbredende materiale
- Er solkilden til alle elementer, og hvordan?
- Er termisk energi en form for energi?
- Hvad er molariteten på 140 g KCl opløst i 600. Ml vand.?
- Målrettet lægemiddellevering med disse nanopartikler kan gøre medicin mere effektiv
- At blive salt:Kan roejuice, andre alternativer være med til at holde landets motorveje isfri?
- Sådan beregnes området af en cirkel med Diameter


