Ionbindinger:Dannelse, elektronoverførsel og iontiltrækning forklaret
En ionbinding dannes, når et metalatom overfører en eller flere elektroner til et ikke-metalatom, hvilket skaber modsat ladede ioner, der tiltrækkes af hinanden.
Her er en oversigt over processen:
1. Elektronoverførsel: Et metalatom, som har en lav ioniseringsenergi, mister let en eller flere elektroner fra sin yderste skal. Dette skaber en positivt ladet ion (kation).
2. Ikke-metal forstærkning: Et ikke-metalatom, som har en høj elektronaffinitet, får let en eller flere elektroner for at færdiggøre sin ydre skal. Dette skaber en negativt ladet ion (anion).
3. Elektrostatisk tiltrækning: De modsatte ladninger af kationen og anionen skaber en stærk elektrostatisk tiltrækning, der holder dem sammen i en stiv krystalgitterstruktur.
Denne overførsel af elektroner resulterer i et stabilt arrangement, hvor begge atomer opnår en fuld ydre skal af elektroner, der opfylder oktetreglen.
Vigtige takeaways:
* Metal og ikke-metal: Ionbindinger opstår mellem metaller og ikke-metaller.
* Elektronoverførsel: Elektroner overføres, deles ikke.
* Modsatte gebyrer: De resulterende ioner har modsatte ladninger og tiltrækker hinanden.
* Krystalgitter: Ionerne danner en stabil, stiv krystalgitterstruktur.
Eksempel: Natrium (Na) og Klor (Cl) reagerer og danner natriumchlorid (NaCl).
* Natrium mister en elektron for at blive en positivt ladet Na+ ion.
* Klor får en elektron til at blive en negativt ladet Cl-ion.
* De modsat ladede ioner tiltrækker og danner den ioniske forbindelse NaCl.
 Varme artikler
Varme artikler
-
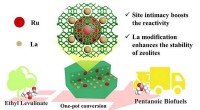 Zeolit-skræddersyet aktiv stednærhed til effektiv produktion af pentanoiske biobrændstofferZeolit-skræddersyet nærhed til aktivt sted øger den katalytiske aktivitet og selektivitet til direkte hydrodeoxygenering af rent ethyllevulinat til pentanoiske biobrændstoffer. Kredit:HE Jiang Ikk
Zeolit-skræddersyet aktiv stednærhed til effektiv produktion af pentanoiske biobrændstofferZeolit-skræddersyet nærhed til aktivt sted øger den katalytiske aktivitet og selektivitet til direkte hydrodeoxygenering af rent ethyllevulinat til pentanoiske biobrændstoffer. Kredit:HE Jiang Ikk -
 Neutroner låser op for egenskaber ved nyt porøst metalhydrid til mulige nye energilagringsapplikat…Stående ved WAND2 instrumentet, forskere (fra venstre mod højre) Michael Heere og Yaroslav Filinchuk med ORNL-strålelinjeforskerne Matthias Frontzek og Simon Kimber. Kredit:ORNL/Jeremy Rumsey Adsk
Neutroner låser op for egenskaber ved nyt porøst metalhydrid til mulige nye energilagringsapplikat…Stående ved WAND2 instrumentet, forskere (fra venstre mod højre) Michael Heere og Yaroslav Filinchuk med ORNL-strålelinjeforskerne Matthias Frontzek og Simon Kimber. Kredit:ORNL/Jeremy Rumsey Adsk -
 Opdagelse inden for cellecyklusproces for at bringe forståelse af cellulære sygdommeEn celle under deling i et lag af celler. Kredit:Åbo Akademi Forskning fra School of Biosciences og University of Manchester har afsløret en væsentlig mekanisme, der koordinerer processerne for ce
Opdagelse inden for cellecyklusproces for at bringe forståelse af cellulære sygdommeEn celle under deling i et lag af celler. Kredit:Åbo Akademi Forskning fra School of Biosciences og University of Manchester har afsløret en væsentlig mekanisme, der koordinerer processerne for ce -
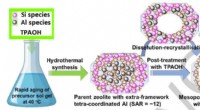 Forskere udvikler hul ZSM-5 zeolitkatalysator med lavt forhold mellem silicium og aluminiumSkematisk illustration af fremstillingen af de mesoporøse ZSM-5-P nanobokse via den hurtige ældning (af precursor sol-gelblandingen) og postsyntetisk TPAOH-behandling. Kredit:IMR ZSM-5 zeolit
Forskere udvikler hul ZSM-5 zeolitkatalysator med lavt forhold mellem silicium og aluminiumSkematisk illustration af fremstillingen af de mesoporøse ZSM-5-P nanobokse via den hurtige ældning (af precursor sol-gelblandingen) og postsyntetisk TPAOH-behandling. Kredit:IMR ZSM-5 zeolit


