Forstå gasvolumen:hvorfor det ikke er løst
Her er en oversigt over hvorfor:
* Gasser er komprimerbare: I modsætning til faste stoffer og væsker er molekylerne i en gas langt fra hinanden. Det betyder, at afstanden mellem gasmolekyler let kan reduceres ved at påføre tryk. Derfor kan volumenet af en gas ændres ved at ændre trykket.
* Gasser udvider sig for at fylde deres beholder: Gasmolekyler bevæger sig tilfældigt og er ikke fikseret i nogen bestemt position. De vil sprede sig for at fylde hele volumen af deres beholder. Dette er grunden til, at gasser ikke har et fast volumen.
Så selvom gas ikke har et fast volumen som et fast stof eller en væske, har den et specifikt volumen ved en given temperatur og tryk. Dette er beskrevet af Ideal Gas Law, som siger:
PV =nRT
Hvor:
* P er tryk
* V er volumen
* n er antallet af mol gas
* R er den ideelle gaskonstant
*T er temperatur
Denne lov viser, at volumenet af en gas er direkte proportional med temperaturen og omvendt proportional med trykket. Derfor kan volumen af en gas beregnes, hvis du kender temperaturen, trykket og mængden af gas.
Sammenfattende har gasser ikke et fast volumen, fordi de er komprimerbare og udvider sig for at fylde deres beholdere. De har dog et bestemt volumen, der afhænger af temperaturen og trykket.
 Varme artikler
Varme artikler
-
 Forskere udvikler en ny metode til forbedring af effektiviteten af luftrensereLuftrenser. Kredit:Sergei Preis, TalTech Ren luft er noget, vi løbende er stolte af i vores lille Estland, og det er blevet kaldt, dels i sjov, en af de vigtigste eksport. Desværre, miljøet, her
Forskere udvikler en ny metode til forbedring af effektiviteten af luftrensereLuftrenser. Kredit:Sergei Preis, TalTech Ren luft er noget, vi løbende er stolte af i vores lille Estland, og det er blevet kaldt, dels i sjov, en af de vigtigste eksport. Desværre, miljøet, her -
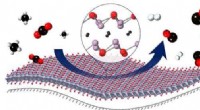 Katalysator for bæredygtig gassynteseEn tynd film af metaloxycarbider på en oxidbærer letter reaktionen mellem CO 2 og methan (CH4) til fremstilling af hydrogen (H2) og kulilte (CO). Kredit:Alexey Kurlov, Evgenia Deeva / ETH Zürich
Katalysator for bæredygtig gassynteseEn tynd film af metaloxycarbider på en oxidbærer letter reaktionen mellem CO 2 og methan (CH4) til fremstilling af hydrogen (H2) og kulilte (CO). Kredit:Alexey Kurlov, Evgenia Deeva / ETH Zürich -
 Bekæmpelse af kræft ved nulpunktet med designermolekylerEn grafisk repræsentation af det nye molekyle (gule pinde), der interagerer med den glidende klemme (grøn overflade). Kredit:University of Adelaide Et nyt molekyle designet af forskere fra Univers
Bekæmpelse af kræft ved nulpunktet med designermolekylerEn grafisk repræsentation af det nye molekyle (gule pinde), der interagerer med den glidende klemme (grøn overflade). Kredit:University of Adelaide Et nyt molekyle designet af forskere fra Univers -
 Hvad afslører abonnementer i kemiske formler?jittawit.21/iStock/GettyImages I hvert kemipensum kondenserer kemiske formler kompleks information til en kompakt notation. Subskripter, der ofte overses, er afgørende – de dikterer den præcise samme
Hvad afslører abonnementer i kemiske formler?jittawit.21/iStock/GettyImages I hvert kemipensum kondenserer kemiske formler kompleks information til en kompakt notation. Subskripter, der ofte overses, er afgørende – de dikterer den præcise samme


