Svovlelektronkonfiguration:At opnå stabilitet og oktetreglen
* Svovls elektronkonfiguration: Svovl har 16 elektroner med følgende konfiguration:2, 8, 6. Det betyder, at det har 6 elektroner i sin yderste skal (valenselektroner).
* Oktetregel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en stabil konfiguration af 8 elektroner i deres yderste skal (oktetreglen).
* Svovls stabilitet: For at opnå en stabil oktet skal svovl få yderligere to elektroner. Dette giver den i alt 8 elektroner i dens yderste skal, hvilket gør den isoelektronisk (med samme elektronkonfiguration) med ædelgassen Argon (Ar).
Derfor får svovl to elektroner for at opnå stabilitet.
Sidste artikelNatrium og svovl:Forståelse af ionisk binding
Næste artikelIdentifikation af forbindelser:Vand vs. blandinger og grundstoffer
 Varme artikler
Varme artikler
-
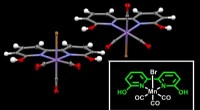 Rekruttering af mangan til at opgradere kuldioxidKrystalstruktur af den manganbaserede katalysator rapporteret i undersøgelsen. Manganatomet (i lilla) er i midten af rammen - liganden - hvilket letter hydrogeneringen af CO2. Kredit:Okinawa Insti
Rekruttering af mangan til at opgradere kuldioxidKrystalstruktur af den manganbaserede katalysator rapporteret i undersøgelsen. Manganatomet (i lilla) er i midten af rammen - liganden - hvilket letter hydrogeneringen af CO2. Kredit:Okinawa Insti -
 Nyt twist i løbet om at udskifte grafitanoden til bedre genopladelige batterierKredit:UC San Diego Jacobs School of Engineering Forbedringer af en klasse af batterielektrolyt, der først blev introduceret i 2017-flydende gaselektrolytter-kunne bane vejen til et kraftigt og læ
Nyt twist i løbet om at udskifte grafitanoden til bedre genopladelige batterierKredit:UC San Diego Jacobs School of Engineering Forbedringer af en klasse af batterielektrolyt, der først blev introduceret i 2017-flydende gaselektrolytter-kunne bane vejen til et kraftigt og læ -
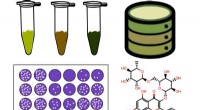 Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch
Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch -
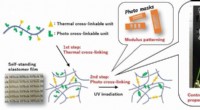 Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk
Udvikling af film med justerbar forlængelse og brud til forskellige formålDobbelt-termisk og foto-tværbinding af polymerkæder til syntese af alsidig elastomer. Forskere fra Japan formåede at udvikle en elastomerfilm med justerbar elasticitet ved hjælp af en to-trins termisk
- Forskere foreslår teknik til måling af svage eller ikke -eksisterende magnetiske felter
- 3-i-1-enhed tilbyder alternativ til Moores lov
- Hvilken proces med ægcelle og sædcelle?
- Hvad danner atomer, når de deler elektroner par?
- Aqua -satellit finder Firenze midlertidigt bekæmpe vindskæring
- Hvilke lag af jorden går en mineskaft igennem?


