Valenselektroner i SF₄²⁻:En trin-for-trin-beregning
1. Valenselektroner af individuelle atomer
* Svovl (S): Svovl er i gruppe 16 (VIA) i det periodiske system, så det har 6 valenselektroner.
* Fluor (F): Fluor er i gruppe 17 (VIIA), så det har 7 valenselektroner.
2. Samlede valenselektroner fra atomer
* Svovl bidrager med 6 elektroner.
* Fire fluoratomer bidrager med 4 * 7 =28 elektroner.
3. Regn for debiteringen
* 2-ladningen betyder, at der er to ekstra elektroner.
4. Samlede valenselektroner
* Samlede valenselektroner =6 + 28 + 2 =36 elektroner
Derfor har SF₄²⁻ 36 valenselektroner.
 Varme artikler
Varme artikler
-
 Hurtig, præcis måde at kontrollere jordnøddeplanter for sunde egenskaberLee Sanchez, medforfatter og biokemi kandidatstuderende, tager jordnøddeprøver til undersøgelsen. Kredit:Dmitry Kurouski Den langvarige proces med at avle bedre jordnøddeplanter kan fremskyndes ve
Hurtig, præcis måde at kontrollere jordnøddeplanter for sunde egenskaberLee Sanchez, medforfatter og biokemi kandidatstuderende, tager jordnøddeprøver til undersøgelsen. Kredit:Dmitry Kurouski Den langvarige proces med at avle bedre jordnøddeplanter kan fremskyndes ve -
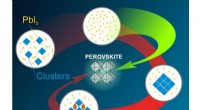 Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b
Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b -
 Hvis bare A.I. havde en hjerne - ingeniører modellerer en kunstig synapse efter den menneskelige hj…Pitt-ingeniører byggede en grafen-baseret kunstig synapse i en todimensionel, bikage -konfiguration af kulstofatomer, der viste fremragende energieffektivitet, der kan sammenlignes med biologiske syna
Hvis bare A.I. havde en hjerne - ingeniører modellerer en kunstig synapse efter den menneskelige hj…Pitt-ingeniører byggede en grafen-baseret kunstig synapse i en todimensionel, bikage -konfiguration af kulstofatomer, der viste fremragende energieffektivitet, der kan sammenlignes med biologiske syna -
 Hurtigere, grønnere måde at producere kulstofkugler påKulissfærer - mikroskopbilleder Hurtig, grøn og et-trins metode til fremstilling af porøse kulstofkugler, som er en vital komponent for kulstoffangstteknologi og for nye måder at lagre vedvarende ener
Hurtigere, grønnere måde at producere kulstofkugler påKulissfærer - mikroskopbilleder Hurtig, grøn og et-trins metode til fremstilling af porøse kulstofkugler, som er en vital komponent for kulstoffangstteknologi og for nye måder at lagre vedvarende ener
- Hvad er en kemisk ændring for blyant?
- Hvornår satte Apollo fod på månen?
- Forskere gør fremskridt inden for nanoteknologiske gensekventeringsteknik
- Hvordan har Gregor Mendel hjulpet med at forme studiet af biologi?
- Hvilken hører svovlvand neon eller kobber, og hvorfor?
- Tidlig kambrisk fossilopdagelse giver ny forståelse for oprindelsen af hemichordater


