Forståelse af ikke-polære kovalente bindinger og elektronegativitet
Her er hvorfor:
* Elektronegativitet: Dette er et atoms evne til at tiltrække elektroner i en binding.
* Polære kovalente bindinger: Når der er en signifikant forskel i elektronegativitet mellem to atomer, trækkes elektronerne i bindingen tættere på det mere elektronegative atom, hvilket skaber en delvis positiv ladning på det ene atom og en delvis negativ ladning på det andet. Dette er en polær kovalent binding.
* Ikke-polære kovalente bindinger: Når de to atomer har lignende elektronegativiteter, deles elektronerne næsten ligeligt. Der er ingen signifikant ladningsadskillelse, hvilket resulterer i en ikke-polær kovalent binding.
Eksempler:
* H₂ (brintgas): Begge brintatomer har samme elektronegativitet, så bindingen er upolær.
* Cl₂ (chlorgas): Begge kloratomer har samme elektronegativitet, så bindingen er upolær.
* O₂ (iltgas): Begge oxygenatomer har samme elektronegativitet, så bindingen er upolær.
Nøgleafhentning: En ikke-polær kovalent binding indikerer, at de to atomer deler elektroner ligeligt, hvilket sker, når deres elektronegativiteter er meget ens.
 Varme artikler
Varme artikler
-
 Forskere er tæt på kræftbehandlinger ved hjælp af CRISPRKredit:CC0 Public Domain Kemoterapi arbejder ud fra en grundlæggende forudsætning:dræb alle hurtigt voksende celler i et forsøg på at udslette tumorceller. Taktikken, selvom det generelt er effekt
Forskere er tæt på kræftbehandlinger ved hjælp af CRISPRKredit:CC0 Public Domain Kemoterapi arbejder ud fra en grundlæggende forudsætning:dræb alle hurtigt voksende celler i et forsøg på at udslette tumorceller. Taktikken, selvom det generelt er effekt -
 Forskere får forskningshydrogel til at vokse mere som biologiske vævForskere fra NTU og CMU skabte en bladlignende hydrogelstruktur gennem en proces, der ligner, hvordan ægte bladvæv vokser. Kredit:CMU og NTU Forskere fra Nanyang Technological University, Singapor
Forskere får forskningshydrogel til at vokse mere som biologiske vævForskere fra NTU og CMU skabte en bladlignende hydrogelstruktur gennem en proces, der ligner, hvordan ægte bladvæv vokser. Kredit:CMU og NTU Forskere fra Nanyang Technological University, Singapor -
 Materialer kemikere banker kropsvarme for at drive smarte beklædningsgenstandeMaterialekemikere ledet af Trisha Andrew ved UMass Amherst har udviklet et stof, der kan høste kropsvarme til at drive små bærbare mikroelektronikker såsom aktivitetsmålere. De producerede og vurdered
Materialer kemikere banker kropsvarme for at drive smarte beklædningsgenstandeMaterialekemikere ledet af Trisha Andrew ved UMass Amherst har udviklet et stof, der kan høste kropsvarme til at drive små bærbare mikroelektronikker såsom aktivitetsmålere. De producerede og vurdered -
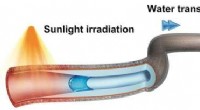 Hurtig kontrolleret transport af vanddråber via sollyspumpeKredit:Wiley Drevet af naturligt eller kunstigt sollys, en ny mikrorørspumpe transporterer vanddråber over lange afstande. Som rapporteret af kinesiske forskere i Journal Angewandte Chemie , pum
Hurtig kontrolleret transport af vanddråber via sollyspumpeKredit:Wiley Drevet af naturligt eller kunstigt sollys, en ny mikrorørspumpe transporterer vanddråber over lange afstande. Som rapporteret af kinesiske forskere i Journal Angewandte Chemie , pum
- Hvad er et eksempel på evolution, der forekommer i dag?
- Hvilke funktioner findes på overfladen af solen?
- Ny SERS-metode udviklet til at fange målmolekyler
- Forskere opdager ny struktur for lovende materialeklasser
- Hvilket navn bruges til at beskrive organismer, der udfører fotosyntesen, gør deres egen madspids?…
- Hvorfor er nogle bjerge skarpe og taggete?


