Stærkeste til svageste vandige baser og syrer:En rangliste
Stærkeste til svageste baser:
1. Natriumhydroxid (NaOH): En stærk base, der dissocierer fuldstændigt i vand og danner hydroxidioner (OH-) og natriumioner (Na+).
2. Ammoniak (NH3): En svag base, der delvist dissocierer i vand og danner ammoniumioner (NH4+) og hydroxidioner (OH-).
3. Calciumhydroxid (Ca(OH)2): En moderat stærk base, der dissocierer til calciumioner (Ca2+) og hydroxidioner (OH-), men ikke fuldstændigt.
Stærkeste til svageste syrer:
1. Saltsyre (HCl): En stærk syre, der dissocierer fuldstændigt i vand og danner hydrogenioner (H+) og chloridioner (Cl-).
2. Eddikesyre (CH3COOH): En svag syre, der delvist dissocierer i vand og danner hydrogenioner (H+) og acetationer (CH3COO-).
3. Kulsyre (H2CO3): En meget svag syre, der dissocierer meget lidt i vand og danner hydrogenioner (H+) og bicarbonationer (HCO3-).
Vigtig bemærkning:
* Styrken af en syre/base er defineret ved dens grad af dissociation i vand. Stærke syrer og baser ioniseres fuldstændigt, mens svage kun delvist ioniseres.
* pH er et mål for surhedsgraden eller alkaliniteten af en opløsning. En lavere pH indikerer en mere sur opløsning, mens en højere pH indikerer en mere basisk opløsning.
Sidste artikelBeregning af atomer i NH₄Cl:En trin-for-trin guide
Næste artikelPlette:En kemisk ændring forklaret | Kemiske reaktioner
 Varme artikler
Varme artikler
-
 Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin
Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin -
 Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love
Video:Hvordan måler vi temperatur?Kredit:The American Chemical Society Vi har stor tillid til, at vi måler temperaturen nøjagtigt. Men hvordan fungerer termometre i køkkenet eller på lægekontoret? Takket være termodynamikkens love -
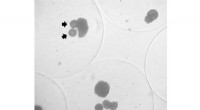 Små lægemiddelleverende kapsler kunne opretholde transplanterede insulinproducerende cellerPancreas-øceller indkapslet sammen med mikrosfærer, der frigiver et lægemiddel, der øger levedygtigheden i miljøer med lavt iltindhold. Mikrosfærerne har pile, der peger på dem; de større klatter er c
Små lægemiddelleverende kapsler kunne opretholde transplanterede insulinproducerende cellerPancreas-øceller indkapslet sammen med mikrosfærer, der frigiver et lægemiddel, der øger levedygtigheden i miljøer med lavt iltindhold. Mikrosfærerne har pile, der peger på dem; de større klatter er c -
 Forståelse af ustabile atomer:ioner, radioaktivitet og atomisk stabilitetAf Chris Deziel, Opdateret 24. marts 2022 kotoffei/iStock/GettyImages TL;DR (for lang; læste ikke) Ioner er elektrisk ustabile og danner hurtigt kemiske bindinger. Atomer med ubalancerede kerner uds
Forståelse af ustabile atomer:ioner, radioaktivitet og atomisk stabilitetAf Chris Deziel, Opdateret 24. marts 2022 kotoffei/iStock/GettyImages TL;DR (for lang; læste ikke) Ioner er elektrisk ustabile og danner hurtigt kemiske bindinger. Atomer med ubalancerede kerner uds


