Omdannelse af jernholdig ascorbat til elementært jern:en detaljeret beregning
Forståelse af kemien
* Jerroaskorbat er en forbindelse, der indeholder jern i sin jernholdige (Fe²⁺) form bundet til ascorbinsyre (vitamin C). Den kemiske formel skrives normalt som Fe(C₆H₇O6)₂.
* Elementært jern er rent jern (Fe) i sin metalliske form.
Beregning
1. Find molekylvægten af ferro-ascorbat:
* Fe:55,845 g/mol
* C:12,011 g/mol
* H:1,008 g/mol
* O:15,999 g/mol
* Molekylvægt af jernholdige ascorbat (Fe(C₆H₇O6)₂) =(55,845 + 12,011 * 12 + 1,008 * 14 + 15,999 * 12) =443,98 g/mol
2. Bestem andelen af jern i jernholdige ascorbat:
* Atomvægt af jern (Fe) / Molekylvægt af jernholdige ascorbat =55,845 g/mol / 443,98 g/mol ≈ 0,126
3. Multipér vægten af jernholdige ascorbat med andelen af jern:
* For eksempel, hvis du har 100 mg jernholdig ascorbat, vil du gange 100 mg * 0,126 =cirka 12,6 mg elementært jern.
Vigtig bemærkning:
* Denne beregning giver den teoretiske ækvivalent af elementært jern i jernholdig ascorbat.
* Biotilgængelighed af jern fra jernholdig ascorbat kan være forskellig fra denne teoretiske værdi, da faktorer som kroppens evne til at optage jern kan variere.
Eksempel:
Hvis et tilskud indeholder 30 mg jernholdige ascorbat, er det tilsvarende elementære jernindhold:
30 mg jernholdige ascorbat * (55,845 g/mol Fe / 443,98 g/mol jernholdige ascorbat) =ca. 3,8 mg elementært jern .
 Varme artikler
Varme artikler
-
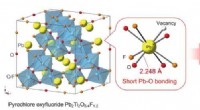 Forskere rapporterer om ny oxyfluoridforbindelse til fotokatalyseIndsatsen viser et billede af Pb 2 Ti 2 O 5 . 4 F 1 . 2 , vist at være i stand til at absorbere synligt lys med en bølgelængde på omkring 500 nm. Denne evne menes at skyldes bindingsstrukt
Forskere rapporterer om ny oxyfluoridforbindelse til fotokatalyseIndsatsen viser et billede af Pb 2 Ti 2 O 5 . 4 F 1 . 2 , vist at være i stand til at absorbere synligt lys med en bølgelængde på omkring 500 nm. Denne evne menes at skyldes bindingsstrukt -
 Formskiftende materiale kan forvandles, vende sig selv ved hjælp af varme, lysKredit:University of Colorado at Boulder Et nyt materiale udviklet af University of Colorado Boulders ingeniører kan forvandle sig til komplekse, forprogrammerede former via lys- og temperaturstim
Formskiftende materiale kan forvandles, vende sig selv ved hjælp af varme, lysKredit:University of Colorado at Boulder Et nyt materiale udviklet af University of Colorado Boulders ingeniører kan forvandle sig til komplekse, forprogrammerede former via lys- og temperaturstim -
 Hold sig kølig:Et almindeligt kølemiddel er lovende for metalgenbrugStetson og Wilson på arbejde i laboratoriet. Kredit:Idaho National Laboratory Det er ikke ualmindeligt i den videnskabelige verden, at en proces har mange unikke anvendelser. For eksempel har forsk
Hold sig kølig:Et almindeligt kølemiddel er lovende for metalgenbrugStetson og Wilson på arbejde i laboratoriet. Kredit:Idaho National Laboratory Det er ikke ualmindeligt i den videnskabelige verden, at en proces har mange unikke anvendelser. For eksempel har forsk -
 Bioingeniører udvikler sig hurtigt, spyt-baseret detektionstest for marihuanaKredit:University of Texas i Dallas Dr. Shalini Prasad (forrest), midlertidig afdelingsleder for bioingeniør ved Erik Jonsson School of Engineering and Computer Science, har den THC-biosensor, som
Bioingeniører udvikler sig hurtigt, spyt-baseret detektionstest for marihuanaKredit:University of Texas i Dallas Dr. Shalini Prasad (forrest), midlertidig afdelingsleder for bioingeniør ved Erik Jonsson School of Engineering and Computer Science, har den THC-biosensor, som
- International forskning gør fremskridt mod forbedrede materialer til kvantesensorteknologi
- Polaroids hjælper videnskabsmænd med at opdage farlig is på flyvemaskiner
- Hvilken proces producerer foldede bjerge?
- Forsker, der studerer havbunden kaldes?
- Hvad er en usædvanlig type bindevæv, fordi det består tæt pakket celler?
- Hvad er magnettråd?


