Forståelse af aktiveringsenergi i kemiske reaktioner
Her er hvorfor:
* Aktiveringsenergi er den mindste mængde energi, som reagerende molekyler skal have for at starte en reaktion.
* Nogle reaktioner kræver meget energi for at komme i gang (som at brænde træ), mens andre let sker ved stuetemperatur (som at ruste).
* Jo højere aktiveringsenergi, jo sværere er det for reaktionen at finde sted.
Faktorer, der påvirker aktiveringsenergien:
* Reaktanternes art: Nogle molekyler er mere reaktive end andre.
* Tilstedeværelse af en katalysator: Katalysatorer fremskynder reaktioner ved at sænke aktiveringsenergien.
* Temperatur: Højere temperaturer øger den kinetiske energi af molekyler, hvilket gør det lettere for dem at overvinde aktiveringsenergibarrieren.
Sig til, hvis du har lyst til at udforske dette nærmere!
 Varme artikler
Varme artikler
-
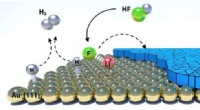 Batteriets skjulte lag afsløretReaktionsmekanismen til omdannelse af hydrogenfluorid (HF) urenhed fra elektrolytten til lithiumfluorid (LiF) i fast-elektrolytinterfasen (SEI) med frigivelse af hydrogengas (H2). SEI -laget er vist p
Batteriets skjulte lag afsløretReaktionsmekanismen til omdannelse af hydrogenfluorid (HF) urenhed fra elektrolytten til lithiumfluorid (LiF) i fast-elektrolytinterfasen (SEI) med frigivelse af hydrogengas (H2). SEI -laget er vist p -
 Katalysatorfremskridt forbedrer naturgasrensningsteknologiKatalysator flåder af palladium (Pd) oxid, der holdes sammen med enkelte atomer af platin, er effektive til at rense emissioner fra naturgasmotorer. Kredit:Cortland Johnson, PNNL. En nyudviklet ka
Katalysatorfremskridt forbedrer naturgasrensningsteknologiKatalysator flåder af palladium (Pd) oxid, der holdes sammen med enkelte atomer af platin, er effektive til at rense emissioner fra naturgasmotorer. Kredit:Cortland Johnson, PNNL. En nyudviklet ka -
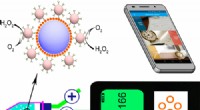 Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr
Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr -
 Innovative transistorer baseret på magnetisk induceret bevægelse af ionerKredit:National Institute for Materials Science Ligesom magneter tiltrækker jernpartikler i sandkasser, permanent magnetik tiltrækker kun én type ion i en elektrokemisk opløsning, udgør grundlaget
Innovative transistorer baseret på magnetisk induceret bevægelse af ionerKredit:National Institute for Materials Science Ligesom magneter tiltrækker jernpartikler i sandkasser, permanent magnetik tiltrækker kun én type ion i en elektrokemisk opløsning, udgør grundlaget
- Er malachit et metal eller ikke metal?
- Sådan kalibreres en gradueret cylinder
- Energien forbundet med den tilfældige vibrationsbevægelse af molekyler.?
- Er elementer blandinger og sammensætning de samme?
- Hvilken ydre planet har en rotrograd rotation?
- Hvordan ændres hydroelektrisk energi til andre nyttige former for energi?


