Permanganatoxidation af klorid:En detaljeret redoxreaktion
Her er den afbalancerede redoxreaktion:
2MnO4-(vandig) + 10Cl-(vandig) + 16H+(vandig) → 2Mn²+(vandig) + 5Cl2(g) + 8H2O(l)
Forklaring:
* Oxidation: Chloridioner (Cl⁻) oxideres til klorgas (Cl2). Hver chloridion mister en elektron for at danne klorgas.
* Reduktion: Permanganationer (MnO4⁻) reduceres til mangan(II)ioner (Mn2+). Hver permanganation får fem elektroner, og dens oxidationstilstand ændres fra +7 til +2.
* Surt medium: Reaktionen kræver et surt medium (H⁺) for at tilvejebringe de nødvendige protoner til reduktion af permanganationer og dannelse af vand.
Betingelser:
* Sur opløsning: Reaktionen forløber let i sure opløsninger, såsom fortyndet svovlsyre.
* Koncentration: Koncentrationen af reaktanterne spiller en rolle i reaktionshastigheden. Højere koncentrationer fører generelt til hurtigere reaktioner.
* Temperatur: Reaktionshastigheden stiger med temperaturen.
Observationer:
* Opløsningen bliver fra lilla (MnO₄⁻) til farveløs (Mn²⁺), når permanganationerne reduceres.
* Den karakteristiske skarpe lugt af klorgas (Cl₂) vil blive observeret.
Bemærk: Denne reaktion er et klassisk eksempel på en redoxreaktion, hvor et stærkt oxidationsmiddel (permanganat) oxiderer et svagere oxidationsmiddel (chlorid).
Sidste artikelNatriumalginatformel og egenskaber:En omfattende guide
Næste artikelKlorsyre (HClO₂):Formel, egenskaber og forklaring
 Varme artikler
Varme artikler
-
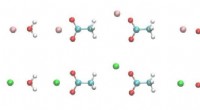 Force field analyse giver spor til protein-ion interaktionStrukturer af metalion-ligand-dimerer. Hvid, cyan, blå, rød, lyserøde og grønne kugler er H, C, N, O, Mg- og Ca -atomer. Kredit:Zhifeng Jing, Rui Qi, Chengwen Liu og Pengyu Ren Muskel rykninger, f
Force field analyse giver spor til protein-ion interaktionStrukturer af metalion-ligand-dimerer. Hvid, cyan, blå, rød, lyserøde og grønne kugler er H, C, N, O, Mg- og Ca -atomer. Kredit:Zhifeng Jing, Rui Qi, Chengwen Liu og Pengyu Ren Muskel rykninger, f -
 Populært nyt byggemateriale hjælper med at måle proteinpartiklerProteinpartikler er ikke sfæriske, selvom nogle af de værktøjer, der bruges til at måle dem, er sfæriske. Kredit:Kelly Irvine/NIST Det er vigtigt at forstå, hvordan proteiner klumper sig sammen i
Populært nyt byggemateriale hjælper med at måle proteinpartiklerProteinpartikler er ikke sfæriske, selvom nogle af de værktøjer, der bruges til at måle dem, er sfæriske. Kredit:Kelly Irvine/NIST Det er vigtigt at forstå, hvordan proteiner klumper sig sammen i -
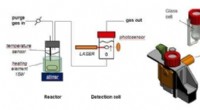 Ny simpel enhed forbedrer analysen af reaktionskinetikken i høj gradBobletællerenheden. Fra venstre til højre:skematisk fremstilling af reaktionskammeret og detektionscellen; ortografisk projektion af detektionscellen og dens hus; og billede af systemet i en praktisk
Ny simpel enhed forbedrer analysen af reaktionskinetikken i høj gradBobletællerenheden. Fra venstre til højre:skematisk fremstilling af reaktionskammeret og detektionscellen; ortografisk projektion af detektionscellen og dens hus; og billede af systemet i en praktisk -
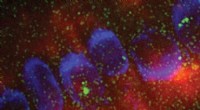 Forskning afslører første bevis på RNA-udløst faseadskillelseKredit:John Innes Center Et grundlæggende spørgsmål i biologi er, hvordan celler orkestrerer kemiske reaktioner i tid og rum. Membranløse organeller er centrum for mange af disse kemiske reaktion
Forskning afslører første bevis på RNA-udløst faseadskillelseKredit:John Innes Center Et grundlæggende spørgsmål i biologi er, hvordan celler orkestrerer kemiske reaktioner i tid og rum. Membranløse organeller er centrum for mange af disse kemiske reaktion
- Hvordan flyver raketten?
- Tilbyder dominansen af den haploide tilstand i en svampe -livscyklus en adaptiv fordel hvorfor eller…
- Hvordan videnskabsmænd over hele verden sporer solcyklussen
- Gaia opdager en spøgelsesgalakse ved siden af
- Ozonniveauet er faldende, men eksponeringen af skove er fortsat høj
- Kan du se en lysstråle i rummet?


