Forståelse af ionproduktet af vand (Kw) - kemi forklaret
Kw =[H3O+][OH-] =1,0 x 10^-14 ved 25°C
Det betyder, at ved 25°C er produktet af koncentrationen af hydroniumion (H3O+) og hydroxidionkoncentrationen (OH-) i rent vand altid lig med 1,0 x 10^-14.
Her er grunden til, at det er vigtigt:
* Forstå surhedsgrad og alkalinitet: Værdien af Kw giver os mulighed for at bestemme, om en opløsning er sur, basisk eller neutral.
* Sure opløsninger: [H3O+]> [OH-]
* Grundlæggende løsninger: [H3O+] <[OH-]
* Neutrale løsninger: [H3O+] =[OH-]
* Beregning af pH og pOH: Kw bruges til at beregne pH og pOH af en opløsning, som er mål for dens surhedsgrad og alkalinitet.
Bemærk: Værdien af Kw ændrer sig lidt med temperaturen.
 Varme artikler
Varme artikler
-
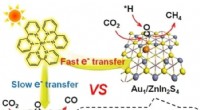 Enkelte guldatomer katalyserer den selektive metanisering af kuldioxidKredit:Wiley Et skridt mod kuldioxid (CO2 ) neutralitet og afbødning af både drivhuseffekten og energikrisen ville være at omdanne CO2 til kulbrintebaserede brændstoffer som metan ved hjælp af lys.
Enkelte guldatomer katalyserer den selektive metanisering af kuldioxidKredit:Wiley Et skridt mod kuldioxid (CO2 ) neutralitet og afbødning af både drivhuseffekten og energikrisen ville være at omdanne CO2 til kulbrintebaserede brændstoffer som metan ved hjælp af lys. -
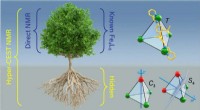 Hyper-CEST NMR-teknik afslører manglende struktur af et nyt beholdermolekyleHyper-CEST som ultrafølsomt NMR-spektroskopiværktøj afslører to tidligere skjulte strukturer af metalorganiske bure. Kredit:Barth van Rossum, FMP Ved hjælp af Hyper-CEST NMR-teknikken har holdet le
Hyper-CEST NMR-teknik afslører manglende struktur af et nyt beholdermolekyleHyper-CEST som ultrafølsomt NMR-spektroskopiværktøj afslører to tidligere skjulte strukturer af metalorganiske bure. Kredit:Barth van Rossum, FMP Ved hjælp af Hyper-CEST NMR-teknikken har holdet le -
 Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio
Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio -
 En smart kemoenzymatisk metode detekterer og fjerner farlige phenolerKredit:CC0 Public Domain Mange industri- og landbrugsprocesser bruger kemikalier, der kan være skadelige for arbejdere og de økosystemer, hvor de ophobes. Forskere fra Thailand har nu udviklet en
En smart kemoenzymatisk metode detekterer og fjerner farlige phenolerKredit:CC0 Public Domain Mange industri- og landbrugsprocesser bruger kemikalier, der kan være skadelige for arbejdere og de økosystemer, hvor de ophobes. Forskere fra Thailand har nu udviklet en
- Biologisk undersøgelse tyder på, at fædres ernæring før sex kan bidrage til babyens sundhed
- Hvilke fysiske faktorer gør et økosystem meget produktivt?
- Hvordan er mangel på ilt relateret til energi?
- Hvor er Hercules konstellationen placeret i himlen?
- Elliott presser på for ændringer på eBay
- Hvilke materialer kommer ind i cellen?


