Jod kovalente bindinger:Forstå bindingsadfærd
Her er hvorfor:
* Valenselektroner: Jod har 7 valenselektroner i sin yderste skal.
* Oktetregel: For at opnå en stabil elektronkonfiguration skal jod få en elektron mere for at fuldføre sin oktet.
* Kovalent binding: Jod opnår dette ved at dele en elektron med et andet atom og danne en enkelt kovalent binding.
Mens jod nogle gange kan danne mere end én binding, er det mest almindeligt at finde det med en enkelt kovalent binding i forbindelser som hydrogeniodid (HI) eller iodmonochlorid (ICl).
Sidste artikelForståelse af pH:Er en pH på 3 sur?
Næste artikelKemiske reaktioner i moderne teknologi:kraft til innovation
 Varme artikler
Varme artikler
-
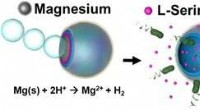 Selvkørende, løglignende mikrokøretøj kan tiltrække, fælde, og ødelægge biologiske truslerKredit:Angewandte Chemie International Edition Antibiotika er mere effektive, når de kan virke på deres mål direkte på angrebsstedet, uden fortynding. I journalen Angewandte Chemie , Amerikanske
Selvkørende, løglignende mikrokøretøj kan tiltrække, fælde, og ødelægge biologiske truslerKredit:Angewandte Chemie International Edition Antibiotika er mere effektive, når de kan virke på deres mål direkte på angrebsstedet, uden fortynding. I journalen Angewandte Chemie , Amerikanske -
 Smuk som en påfugl:Ædelstenen til næste generation af smarte sensorerKredit:CC0 Public Domain Forskere har hentet inspiration fra biomimik af sommerfuglevinger og påfuglefjer for at udvikle et innovativt opallignende materiale, der kunne være hjørnestenen i næste g
Smuk som en påfugl:Ædelstenen til næste generation af smarte sensorerKredit:CC0 Public Domain Forskere har hentet inspiration fra biomimik af sommerfuglevinger og påfuglefjer for at udvikle et innovativt opallignende materiale, der kunne være hjørnestenen i næste g -
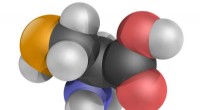 Ny dyb-læringstilgang forudsiger proteinstruktur fra aminosyresekvensAminosyren selenocystein, 3D-bolde model. Kredit:YassineMrabet/CC BY 3.0/Wikipedia Næsten alle grundlæggende biologiske processer, der er nødvendige for liv, udføres af proteiner. De skaber og ved
Ny dyb-læringstilgang forudsiger proteinstruktur fra aminosyresekvensAminosyren selenocystein, 3D-bolde model. Kredit:YassineMrabet/CC BY 3.0/Wikipedia Næsten alle grundlæggende biologiske processer, der er nødvendige for liv, udføres af proteiner. De skaber og ved -
 Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f
Molekylær lim gør perovskite solceller dramatisk mere pålidelige over tidForskere har brugt selvsamlet monolags molekylær lim til at styrke grænseflader i perovskite solceller for at gøre dem mere effektive, stabil og pålidelig. Kredit:Padture lab/Brown University Et f
- Hvilken type bølger kræver ikke stof for at bære energi?
- Hvilke kriterier bruges til klassificering af menneskelige racer?
- I reaktionen mellem brom og natrium får et atom en elektron og danner ion Br. hvad sker der med bro…
- Gliaceller forklaret:typer, funktioner og deres rolle i nervesystemet
- Drivhusgasdata dybt dyk når nyt niveau af rimeligt og sandt
- Identificer de organismer, der også kaldes kopdyr?


