Empirisk vs. molekylær formel:Forstå forskellen
Empirisk formel
* Definition: Det enkleste hele talforhold mellem atomer i en forbindelse. Den fortæller dig, hvilke typer atomer der er til stede og deres relative proportioner.
* Eksempel: Den empiriske formel for glucose (C₆H₁₂O6) er CH₂O, fordi forholdet mellem carbon-, hydrogen- og oxygenatomer er 1:2:1.
* Fokus: Giver de mest grundlæggende oplysninger om sammensætningen af en forbindelse.
* Begrænsninger: Afslører ikke det faktiske antal atomer i et molekyle, kun deres relative forhold.
Molekylær formel
* Definition: Det faktiske antal af hver type atom til stede i et molekyle af forbindelsen.
* Eksempel: Den molekylære formel for glucose er C₆H₁₂O6, hvilket præcist afspejler, at hvert molekyle indeholder seks carbonatomer, tolv hydrogenatomer og seks oxygenatomer.
* Fokus: Giver det komplette billede af atomerne og deres arrangement i et molekyle.
* Forhold til empiri: Den molekylære formel er et multiplum af den empiriske formel. For eksempel har glucose (C₆H₁₂O6) en molekylformel, der er seks gange større end dens empiriske formel (CH2O).
I oversigt
Tænk på det sådan her:
* Empirisk formel: Som en plan, der viser de grundlæggende byggesten i en struktur.
* Molekylformel: Som en detaljeret arkitektonisk plan, der viser den nøjagtige størrelse og arrangement af alle materialer i strukturen.
Hvornår skal du bruge hver:
* Empirisk formel: Nyttigt ved bestemmelse af det enkleste forhold mellem atomer i en forbindelse, ofte brugt i analytisk kemi.
* Molekylformel: Væsentligt, når man skal forstå strukturen og egenskaberne af et molekyle, brugt flittigt i organisk kemi og biokemi.
Sidste artikelEmpirisk vs. molekylær formel:Kan de være de samme?
Næste artikelForståelse af saltsyrefarer:Hvorfor advarselsmærkatet?
 Varme artikler
Varme artikler
-
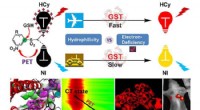 Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning
Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning -
 Min ambition? En anden nobelpris siger kemipristagerCharpentier modtog sit Nobeldiplom og medalje af Per Thoresson, den svenske ambassadør i Tyskland, i Berlin på mandag At vinde Nobelprisen er ofte toppen af professionel præstation, men kemipris
Min ambition? En anden nobelpris siger kemipristagerCharpentier modtog sit Nobeldiplom og medalje af Per Thoresson, den svenske ambassadør i Tyskland, i Berlin på mandag At vinde Nobelprisen er ofte toppen af professionel præstation, men kemipris -
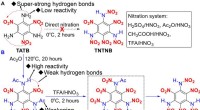 Syntese af TNTNB repræsenterer ny energitop for organiske sprængstofferSyntese af TNTNB.(A) Mislykket nitrering fra TATB til TNTNB ved brug af forskellige nitreringssystemer. (B) Syntese af TNTNB under anvendelse af den foreslåede acylerings-aktiverings-nitreringsstrateg
Syntese af TNTNB repræsenterer ny energitop for organiske sprængstofferSyntese af TNTNB.(A) Mislykket nitrering fra TATB til TNTNB ved brug af forskellige nitreringssystemer. (B) Syntese af TNTNB under anvendelse af den foreslåede acylerings-aktiverings-nitreringsstrateg -
 Flyt over Rover:Der er et nyt snusende kraftcenter i nabolagetElefanten Kelly leder efter mad over øjenhøjde ved hjælp af sin snabel. Kredit:Thomas Spencer, CC-BY Nogle dyr har en superkraft i deres lugtesans. De udforsker, fortolke og forstå deres verden me
Flyt over Rover:Der er et nyt snusende kraftcenter i nabolagetElefanten Kelly leder efter mad over øjenhøjde ved hjælp af sin snabel. Kredit:Thomas Spencer, CC-BY Nogle dyr har en superkraft i deres lugtesans. De udforsker, fortolke og forstå deres verden me
- Er det, når det forbliver uændret i nærvær af nitrogen kemisk eller fysisk?
- Hvilken tilpasning vil sandsynligvis hjælpe prærietræer med at modstå en brand?
- Er glas, der smelter en kemisk ændring?
- Ved hjælp af virkelige data, forskere besvarer nøglespørgsmål om en atmosfærisk udslip
- NASA lukker Chamber A-døren for at påbegynde Webb-teleskoptest
- Hvad kaldes en miljøforsker?


