Ionbinding forklaret:Elektronoverførsel og forskelle fra kovalente bindinger
Ionbinding involverer overførsel af en eller flere elektroner fra et atom til et andet. Dette er den vigtigste forskel, der fører til dannelsen af ioner (atomer med en netto positiv eller negativ ladning).
vand (H2O) er dog ikke et godt eksempel på ionbinding. Vand dannes gennem kovalent binding, hvor atomer deler elektroner i stedet for at overføre dem.
Her er en oversigt:
* Ionisk binding:
* Forekommer mellem metaller (som har tendens til at miste elektroner) og ikke-metaller (som har tendens til at få elektroner).
* Medfører dannelse af ioner med modsatte ladninger.
* Eksempel:Natriumchlorid (NaCl) - Natrium mister en elektron for at blive en positiv ion (Na+), og klor får en elektron til at blive en negativ ion (Cl-). Den stærke elektrostatiske tiltrækning mellem disse modsat ladede ioner danner ionbindingen.
* Kovalent binding:
* Forekommer mellem ikke-metaller.
* Indebærer deling af elektroner mellem atomer.
* Eksempel:Vand (H₂O) - Hvert brintatom deler en elektron med oxygenatomet for at danne et stabilt molekyle.
Sig til, hvis du har flere spørgsmål!
 Varme artikler
Varme artikler
-
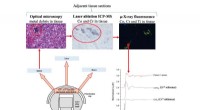 Undersøgelse af metalaflejring i organer efter ledudskiftningFigur 1:Oversigt over undersøgelsen. Kredit:Diamond Light Source Hofteprotesen anses for at være en af de mest vellykkede ortopædiske indgreb, med 75, 000 udført hvert år af NHS alene. Imidlerti
Undersøgelse af metalaflejring i organer efter ledudskiftningFigur 1:Oversigt over undersøgelsen. Kredit:Diamond Light Source Hofteprotesen anses for at være en af de mest vellykkede ortopædiske indgreb, med 75, 000 udført hvert år af NHS alene. Imidlerti -
 Trin-for-trin guide til tegning af en calciumchlorid-skalmodelAf Susan Elliott | Opdateret 30. august 2022 Billede: Forbindelser kan se simple ud, men de er resultatet af komplekse interaktioner på atomniveau. En skalmodel visualiserer disse interaktioner og a
Trin-for-trin guide til tegning af en calciumchlorid-skalmodelAf Susan Elliott | Opdateret 30. august 2022 Billede: Forbindelser kan se simple ud, men de er resultatet af komplekse interaktioner på atomniveau. En skalmodel visualiserer disse interaktioner og a -
 Fra kontorvinduer til Mars:Forskere debuterer med superisolerende gelQingkun Liu, en postdoktoral forskningsassistent ved CU Boulder, holder prøver af en ny gel, der kan forbedre energieffektiviteten af vinduer i hele USA. Kredit:CU Boulder En ny, superisolerende
Fra kontorvinduer til Mars:Forskere debuterer med superisolerende gelQingkun Liu, en postdoktoral forskningsassistent ved CU Boulder, holder prøver af en ny gel, der kan forbedre energieffektiviteten af vinduer i hele USA. Kredit:CU Boulder En ny, superisolerende -
 Cryo-EM-strukturer af nikotinreceptoren kan føre til nye terapier for afhængighedTredimensionelle strukturer af nikotinacetylcholinreceptor bestemt af cryo-EM, med tilladelse fra Hibbs Lab. Kredit:Hibbs Lab, UT Southwestern Medical Center UT Southwestern forskere offentliggjor
Cryo-EM-strukturer af nikotinreceptoren kan føre til nye terapier for afhængighedTredimensionelle strukturer af nikotinacetylcholinreceptor bestemt af cryo-EM, med tilladelse fra Hibbs Lab. Kredit:Hibbs Lab, UT Southwestern Medical Center UT Southwestern forskere offentliggjor


