Beregning af mol af ammoniak:en trin-for-trin guide
1. Hvis du har massen af ammoniak:
* Find den molære masse af ammoniak (NH₃):
* Nitrogen (N) har en molær masse på 14,01 g/mol.
* Brint (H) har en molær masse på 1,01 g/mol.
* Total molær masse af NH3 =14,01 + (3 * 1,01) =17,04 g/mol
* Del ammoniakmassen med dens molære masse:
* Mol ammoniak =(masse af ammoniak i gram) / (17,04 g/mol)
2. Hvis du har mængden af ammoniak (som en gas):
* Du skal kende temperaturen og trykket af ammoniakgassen.
* Brug den ideelle gaslov: PV =nRT
* P =tryk (i atm)
* V =volumen (i liter)
* n =antal mol
* R =ideel gaskonstant (0,0821 L·atm/mol·K)
* T =temperatur (i Kelvin)
* Omarranger ligningen for at løse for n (antal mol):
* n =(PV) / (RT)
Eksempel:
Lad os sige, at du har 0,75 gram af ammoniak.
* Mol ammoniak =(0,75 g) / (17,04 g/mol) ≈ 0,044 mol
Angiv venligst massen eller volumen af ammoniak, så kan jeg beregne antallet af mol for dig.
Sidste artikelGåde:Hvilken farveløs væske starter med W? - Mulige svar
Næste artikelKobbersulfat krystaldannelse:Forståelse af CuSO₄·5H₂O
 Varme artikler
Varme artikler
-
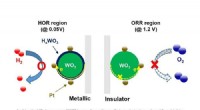 Forskere løser et holdbarhedsproblem i brændselsceller til brintbilerKredit:Pohang University of Science &Technology (POSTECH) Når en cykel bliver våd i regnen, rammen og kæden bliver tæret eller rusten, hvilket forkorter cyklens levetid. Der skal regelmæssigt påfø
Forskere løser et holdbarhedsproblem i brændselsceller til brintbilerKredit:Pohang University of Science &Technology (POSTECH) Når en cykel bliver våd i regnen, rammen og kæden bliver tæret eller rusten, hvilket forkorter cyklens levetid. Der skal regelmæssigt påfø -
 Divalent guldkompleks isoleret for første gang i ren formGuld i sin divalente form er stabilt i midten af porfyriner. Kredit:Katja Heinze, JGU Ifølge lærebogsviden, de sædvanlige oxidationstilstande for guld i forbindelser er +I og +III. Den divalente
Divalent guldkompleks isoleret for første gang i ren formGuld i sin divalente form er stabilt i midten af porfyriner. Kredit:Katja Heinze, JGU Ifølge lærebogsviden, de sædvanlige oxidationstilstande for guld i forbindelser er +I og +III. Den divalente -
 Mantis rejer dactyl køller kunne rumme hemmeligheder til mere modstandsdygtige overflader til menne…Kredit:Unsplash/CC0 Public Domain University of California, Irvines materialevidenskabsforskere lærer om modstandsdygtighed fra mantis-rejen. De gamle krebsdyr er bevæbnet med to hammerlignende ra
Mantis rejer dactyl køller kunne rumme hemmeligheder til mere modstandsdygtige overflader til menne…Kredit:Unsplash/CC0 Public Domain University of California, Irvines materialevidenskabsforskere lærer om modstandsdygtighed fra mantis-rejen. De gamle krebsdyr er bevæbnet med to hammerlignende ra -
 Forskere udvikler ny chip til hurtig og præcis sygdomsopdagelse til lave omkostningerNUS Engineering-forskere har udviklet en billig microfluid-chip, der hurtigt og præcist kan detektere og kvantificere nano-biopartikler ved hjælp af kun et standard laboratoriemikroskop uden fluoresce
Forskere udvikler ny chip til hurtig og præcis sygdomsopdagelse til lave omkostningerNUS Engineering-forskere har udviklet en billig microfluid-chip, der hurtigt og præcist kan detektere og kvantificere nano-biopartikler ved hjælp af kun et standard laboratoriemikroskop uden fluoresce
- Navngiv de 2 humane gameter og fortæl deres kromosomnummer?
- Hvordan modulerer du tyngdekraftsbølger?
- Hvorfor træ fyrer af pop og knitren:Videnskaben bag lyden
- Hvordan relaterer frekvensen til bølgeenergi?
- Hvad er den type kredsløb, hvor to pærer ligger ved siden af hinanden?
- Hvor mange gange kan Pluto passe ind i Jupiter?


