Platin og hydrogenperoxid:Katalytisk nedbrydning forklaret
* Platin som katalysator: Platin er en yderst effektiv katalysator til nedbrydning af hydrogenperoxid. Katalysatorer fremskynder kemiske reaktioner uden at blive forbrugt selv.
* Reaktionen:
* 2 H2O2 (hydrogenperoxid) → 2 H2O (vand) + O2 (iltgas)
* Hvad sker der:
* Platin giver en overflade, hvor hydrogenperoxidmolekyler let kan adsorbere (hæfte sig).
* Denne adsorption svækker bindingerne i hydrogenperoxidmolekylet, hvilket gør det lettere for molekylet at bryde fra hinanden.
* Nedbrydningen af brintoverilte frigiver iltgas, som du ville se som bobler, der dannes i opløsningen.
Observationer:
* Du vil observere bobler som iltgas frigives.
* Løsningen kan skumme eller skum afhængig af koncentrationen af hydrogenperoxid og mængden af platin.
* Reaktionen vil generere varme , hvilket indikerer en eksoterm proces.
Sikkerhed:
* Hydrogenperoxid er et stærkt oxidationsmiddel, og dets nedbrydning kan være kraftig, især med en katalysator.
* Håndter brintoverilte med forsigtighed og bære passende sikkerhedsudstyr.
* Brug ikke store mængder hydrogenperoxid eller platin i en lille beholder, da reaktionen kan blive ukontrollerbar.
Bemærk: Reaktionen er ikke en simpel kemisk reaktion hvor platin bare reagerer med brintoverilte. Platinet fungerer som en overflade til nedbrydning af hydrogenperoxidmolekyler, hvilket fremskynder processen uden at ændre dens kemiske sammensætning.
Sidste artikelZink- og HCl-reaktion:Balanceret ligning og forklaring
Næste artikelJern(III)chlorid (FeCl3):Forståelse af ionbindingen
 Varme artikler
Varme artikler
-
 Lactase forklaret:dens enzymklasse og rolle i laktosefordøjelseHvis en skål is får dig til at føle dig oppustet, kan synderen være mangel på laktase, enzymet, der nedbryder laktose til fordøjelige sukkerarter. Mens de fleste spædbørn og mange voksne – især de af
Lactase forklaret:dens enzymklasse og rolle i laktosefordøjelseHvis en skål is får dig til at føle dig oppustet, kan synderen være mangel på laktase, enzymet, der nedbryder laktose til fordøjelige sukkerarter. Mens de fleste spædbørn og mange voksne – især de af -
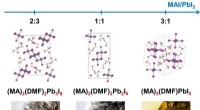 Forskere foreslår metode til at øge effektiviteten af solcellebatterierKrystalstrukturer af krystallinske solvater. Kredit:Alexey Tarasov Forskere fra Institut for Materialevidenskab, Lomonosov MSU, har bestemt, hvordan ændring af forholdet mellem komponenter, der da
Forskere foreslår metode til at øge effektiviteten af solcellebatterierKrystalstrukturer af krystallinske solvater. Kredit:Alexey Tarasov Forskere fra Institut for Materialevidenskab, Lomonosov MSU, har bestemt, hvordan ændring af forholdet mellem komponenter, der da -
 Hvorfor et nysgerrigt krebsdyr kunne holde hemmeligt for at lave vedvarende energi fra træGribble på et stykke træ. Kredit:Claire Steele-King og Katrin Besser, University of York Forskere, der studerer fordøjelsessystemet hos et nysgerrigt træædende krebsdyr, har opdaget, at det kan væ
Hvorfor et nysgerrigt krebsdyr kunne holde hemmeligt for at lave vedvarende energi fra træGribble på et stykke træ. Kredit:Claire Steele-King og Katrin Besser, University of York Forskere, der studerer fordøjelsessystemet hos et nysgerrigt træædende krebsdyr, har opdaget, at det kan væ -
 Tegn-selv-elektroder sat til at fremskynde udviklingen af mikrodetektionsenhederEn Iron-Man-formet elektrode trykt ved hjælp af teknikken. Kredit:Imperial College London Miniatureanordninger til sansning af biologiske molekyler kunne udvikles hurtigere takket være en hurtig p
Tegn-selv-elektroder sat til at fremskynde udviklingen af mikrodetektionsenhederEn Iron-Man-formet elektrode trykt ved hjælp af teknikken. Kredit:Imperial College London Miniatureanordninger til sansning af biologiske molekyler kunne udvikles hurtigere takket være en hurtig p


