Intermolekylære kræfter:F2 vs. Cl2 - Hvilken er stærkere?
Her er hvorfor:
* London Dispersion Forces: Både F₂ og Cl₂ er upolære molekyler, så de eneste intermolekylære kræfter, de oplever, er London-spredningskræfter. Disse kræfter opstår fra midlertidige fluktuationer i elektronfordelingen i molekylet, hvilket skaber midlertidige dipoler.
* Størrelse og polariserbarhed: Kloratomer er større end fluoratomer. Større atomer har flere elektroner, og disse elektroner er længere væk fra kernen. Dette gør dem mere polariserbare, hvilket betyder, at deres elektronskyer lettere kan forvrænges for at skabe midlertidige dipoler.
* Styrke af London Dispersion Forces: Større, mere polariserbare molekyler har stærkere London-spredningskræfter. Da Cl₂ er større og mere polariserbar end F₂, er dens London-spredningskræfter stærkere.
Opsummering: De stærkere London-spredningskræfter i Cl₂ på grund af dens større størrelse og større polariserbarhed gør, at den har stærkere intermolekylære kræfter end F₂.
Sidste artikelEnzymer:Forståelse af deres rolle i biokemiske reaktioner
Næste artikelAmmoniumkogepunkt:Forståelse af ioniske forbindelser
 Varme artikler
Varme artikler
-
 At studere virale udbrud i enkeltceller kan afsløre nye måder at besejre dem påKredit:CC0 Public Domain Mange vira, herunder hiv og influenza A, muterer så hurtigt, at identifikation af effektive vacciner eller behandlinger er som at forsøge at ramme et bevægeligt mål. En be
At studere virale udbrud i enkeltceller kan afsløre nye måder at besejre dem påKredit:CC0 Public Domain Mange vira, herunder hiv og influenza A, muterer så hurtigt, at identifikation af effektive vacciner eller behandlinger er som at forsøge at ramme et bevægeligt mål. En be -
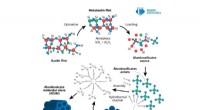
 Ny teknik omdanner problemfrit ammoniak til grøn brintKredit:CC0 Public Domain Northwestern University forskere har udviklet en yderst effektiv, miljøvenlig metode til at omdanne ammoniak til brint. Skitseret i en nylig publikation i tidsskriftet Jo
Ny teknik omdanner problemfrit ammoniak til grøn brintKredit:CC0 Public Domain Northwestern University forskere har udviklet en yderst effektiv, miljøvenlig metode til at omdanne ammoniak til brint. Skitseret i en nylig publikation i tidsskriftet Jo -
 Elektronmikroskopi giver fingerpeg om den farverige kemi af guldsmedevingerDen strålende vingeglans af den hanlige Amazonas guldsmede, Chalcopteryx rutilans, får det kaldenavnet glittervinge, og er genstand for en undersøgelse af farvemekanisme. Kredit:Science and Technology
Elektronmikroskopi giver fingerpeg om den farverige kemi af guldsmedevingerDen strålende vingeglans af den hanlige Amazonas guldsmede, Chalcopteryx rutilans, får det kaldenavnet glittervinge, og er genstand for en undersøgelse af farvemekanisme. Kredit:Science and Technology -
 Kemiker skaber katalysator til at producere anti-mygstofferKredit:RUDN University En kemiker fra RUDN University har udviklet en katalysator til produktion af eugenolacetat, et stof, der ødelægger myggens larver, der overfører farlige sygdomme. Artiklen b
Kemiker skaber katalysator til at producere anti-mygstofferKredit:RUDN University En kemiker fra RUDN University har udviklet en katalysator til produktion af eugenolacetat, et stof, der ødelægger myggens larver, der overfører farlige sygdomme. Artiklen b
- Hvor meget kaliumnitrat skal opløses i vand absorberer 107 kJ varme?
- Hvordan er inerti relateret til objektermassen?
- Den globale opvarmning kan være det dobbelte af, hvad klimamodeller forudsiger
- Hvor mange typer system er der i menneskelig krop?
- Høj risiko for virksomhedskonkurs på grund af coronavirus-pandemien, ifølge en ny analyse
- Kan du blive tosidig senere i livet? Det kommer an på


