Eddikesyre og natriumacetat som bufferopløsning:kemi forklaret
Sådan virker det:
* Eddikesyre (CH3COOH) er en svag syre. Den ioniserer kun delvist i vand, hvilket betyder, at den ikke let donerer alle sine hydrogenioner (H+).
* Natriumacetat (CH3COONa) er saltet af eddikesyre. Det dissocierer fuldstændigt i vand og giver acetationer (CH3COO-).
Bufferhandling:
1. Modstand mod pH-ændringer fra tilsat syre: Hvis du tilføjer en stærk syre (som HCl) til bufferen, reagerer acetat-ionerne (CH3COO-) fra natriumacetatet med de tilsatte H+-ioner og danner eddikesyre (CH3COOH). Denne reaktion forbruger det tilsatte H+, hvilket forhindrer et betydeligt fald i pH.
CH3COO- + H+ ⇌ CH3COOH
2. Modstand mod pH-ændringer fra tilføjet base: Hvis du tilføjer en stærk base (som NaOH) til bufferen, reagerer eddikesyren (CH3COOH) med de tilsatte OH-ioner og danner acetationer (CH3COO-) og vand (H2O). Denne reaktion forbruger den tilsatte OH-, hvilket forhindrer en betydelig stigning i pH.
CH3COOH + OH- ⇌ CH3COO- + H2O
Nøglepunkter:
* Bufferkapacitet: Bufferen kan modstå pH-ændringer inden for et vist område, bestemt af koncentrationerne af den svage syre og dens konjugerede base (acetationer i dette tilfælde).
* pH i bufferen: Bufferopløsningens pH kan beregnes ved hjælp af Henderson-Hasselbalch-ligningen, som tager hensyn til pKa af den svage syre og forholdet mellem koncentrationerne af syren og dens konjugerede base.
Opsummering:
Eddikesyre/natriumacetat-buffersystemet modstår effektivt ændringer i pH ved at reagere med tilsatte syrer eller baser og opretholder en relativt stabil pH inden for et specifikt område. Dette gør det nyttigt i applikationer, hvor pH-kontrol er kritisk, såsom i biologiske systemer eller kemiske reaktioner.
 Varme artikler
Varme artikler
-
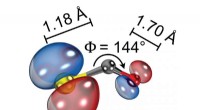 Bestemmelse af strukturen af et molekyle med laserinduceret elektrondiffraktionSkematisk illustration af den molekylære struktur af ioniseret carbonylsulfid (OCS + ) viser dens bøjede og asymmetriske konfiguration og bindingslængderne mellem atomer. Kredit:ICFO Lysmikrosko
Bestemmelse af strukturen af et molekyle med laserinduceret elektrondiffraktionSkematisk illustration af den molekylære struktur af ioniseret carbonylsulfid (OCS + ) viser dens bøjede og asymmetriske konfiguration og bindingslængderne mellem atomer. Kredit:ICFO Lysmikrosko -
 Nye biomaterialer kan finjusteres til medicinske anvendelserKredit:Unsplash/CC0 Public Domain Det er lykkedes forskere i Storbritannien og USA at finjustere et nyt termoplastisk biomateriale, så både den hastighed, hvormed det nedbrydes i kroppen, og dets
Nye biomaterialer kan finjusteres til medicinske anvendelserKredit:Unsplash/CC0 Public Domain Det er lykkedes forskere i Storbritannien og USA at finjustere et nyt termoplastisk biomateriale, så både den hastighed, hvormed det nedbrydes i kroppen, og dets -
 Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo
Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo -
 Durian hudbiokomposit til udtagningsbeholdere og 3D-printDurian er en frugt, der almindeligvis findes i hele Sydøstasien med et meget tykt og frugtigt ydre. Kredit:Kalai via Wikimedia Forskere ved Det Internationale Islamiske Universitet Malaysia har ud
Durian hudbiokomposit til udtagningsbeholdere og 3D-printDurian er en frugt, der almindeligvis findes i hele Sydøstasien med et meget tykt og frugtigt ydre. Kredit:Kalai via Wikimedia Forskere ved Det Internationale Islamiske Universitet Malaysia har ud


