Natrium (Na+) vs. Chlorid (Cl-) ioner:Dannelse, egenskaber og symboler
Kontrast af natrium- og kloridioner
Her er en opdeling af forskellene mellem natrium- og chloridioner, herunder deres dannelse:
Natriumion (Na+)
* Formation: Natrium (Na) er et metal med en elektron i sin yderste skal. Den mister let denne elektron for at opnå en stabil oktetkonfiguration og bliver til en positivt ladet ion (kation). Denne proces kaldes ionisering.
* Symbol: Na+
* Egenskaber:
* Lille størrelse
* Høj ladningstæthed
* Meget reaktiv, danner let ionbindinger
Chloridion (Cl-)
* Formation: Klor (Cl) er et ikke-metal med syv elektroner i sin yderste skal. Den får en elektron til at opnå en stabil oktetkonfiguration, der bliver en negativt ladet ion (anion).
* Symbol: Cl-
* Egenskaber:
* Større størrelse end natriumion
* Lavere ladningstæthed
* Mindre reaktiv sammenlignet med natriumion
Nøgleforskelle:
* Debitering: Natriumion er positivt ladet (Na+), mens chloridion er negativt ladet (Cl-).
* Formation: Natrium mister en elektron for at danne en kation, mens klor får en elektron til at danne en anion.
* Størrelse: Natriumion er mindre end chloridion.
* Reaktivitet: Natriumion er mere reaktivt end chloridion.
Sådan dannes de:
Natrium- og kloratomer danner en ionbinding. Denne binding dannes på grund af den elektrostatiske tiltrækning mellem de modsat ladede ioner. Når et natriumatom (Na) interagerer med et kloratom (Cl), mister natriumatomet sin yderste elektron til kloratomet. Natriumatomet bliver til en positivt ladet natriumion (Na+), og chloratomet bliver til en negativt ladet chloridion (Cl-). Disse modsat ladede ioner tiltrækker hinanden og danner den ioniske forbindelse natriumchlorid (NaCl) eller bordsalt.
Opsummering:
Natrium- og chloridioner er væsentlige komponenter i mange biologiske processer og har forskellige egenskaber på grund af deres forskellige dannelsesprocesser og ladning. Deres interaktion fører til dannelsen af ioniske forbindelser som natriumchlorid, som spiller en afgørende rolle i vores liv.
 Varme artikler
Varme artikler
-
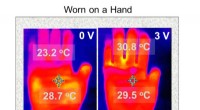 Elektrisk opvarmede tekstiler nu muligtEn tre-lags handske udviklet af materialekemiker Trisha Andrew har et lag belagt med den ledende polymer PEDOT og er drevet af et knapbatteri, der vejer 1,8 gram. Kredit:UMass Amherst Pendlere, sk
Elektrisk opvarmede tekstiler nu muligtEn tre-lags handske udviklet af materialekemiker Trisha Andrew har et lag belagt med den ledende polymer PEDOT og er drevet af et knapbatteri, der vejer 1,8 gram. Kredit:UMass Amherst Pendlere, sk -
 Grønt lys for en ny generation af dynamiske materialerForskere ved QUT, UGent og KIT har været banebrydende for et nyt TAD/naphthalen-baseret lysstabiliseret dynamisk materiale, der er stabilt under synligt grønt lys og bliver flydende over tid i mørke.
Grønt lys for en ny generation af dynamiske materialerForskere ved QUT, UGent og KIT har været banebrydende for et nyt TAD/naphthalen-baseret lysstabiliseret dynamisk materiale, der er stabilt under synligt grønt lys og bliver flydende over tid i mørke. -
 LED-vej:En ren og bekvem metode til at oxidere plastoverflader til industrienFig. 1:Surface oxygenering af sidekædede methylgrupper i polypropylen under fotobestråling med chlordioxid. Kredit:Osaka University Polypropylen (PP) er overalt, er en af de mest anvendte plastm
LED-vej:En ren og bekvem metode til at oxidere plastoverflader til industrienFig. 1:Surface oxygenering af sidekædede methylgrupper i polypropylen under fotobestråling med chlordioxid. Kredit:Osaka University Polypropylen (PP) er overalt, er en af de mest anvendte plastm -
 Eksperimentel vaccine sløver den dødeligste af syntetiske opioiderPotentielt dødelige doser af fentanyl og carfentanil er en brøkdel af dødelige mængder heroin, hvilket har udløst en alarmerende stigning i overdosisdødsfald. Kredit:U.S. Attorneys Office Da opioi
Eksperimentel vaccine sløver den dødeligste af syntetiske opioiderPotentielt dødelige doser af fentanyl og carfentanil er en brøkdel af dødelige mængder heroin, hvilket har udløst en alarmerende stigning i overdosisdødsfald. Kredit:U.S. Attorneys Office Da opioi
- Hvad er et mini -organ, der hjælper cellen med at udføre visse funktioner?
- Sådan beregnes en bølgelængde i Balmer-serien
- Kunstig intelligens møder materialevidenskab
- Hvad er en god videnskabelig fair titel, der beskæftiger sig med Star Life Cycle?
- Udsender galaksen lys eller reflekterer lys?
- Undersøgelse af, hvordan sollys nedbryder plastik på havets overflade


