Guld og saltsyre:Kemisk reaktion og hvorfor guld ikke opløses
Her er hvorfor:
* Guld er et ædelt metal: Det er meget ureaktivt på grund af dets stabile elektronkonfiguration.
* Saltsyre er et svagt oxidationsmiddel: Det er ikke stærkt nok til at oxidere guld og bryde dets kemiske bindinger.
For at opløse guld skal du bruge et stærkere oxidationsmiddel. Dette opnås gennem en proces kaldet aqua regia , som er en stærkt ætsende blanding af koncentreret salpetersyre og saltsyre, optimalt i et molforhold på 1:3.
I aqua regia:
* Salpetersyre fungerer som oxidationsmiddel: Det oxiderer guldioner ($Au^{3+}$) fra guldmetallet.
* Saltsyre reagerer med guldionerne: Det danner tetrachloraurat(III)-anioner ($[AuCl_4]^−$), som er opløselige i opløsning.
Reaktionen i aqua regia kan opsummeres som følger:
$Au + 3 HNO_3 + 4 HCl \longrightpil [AuCl_4]^- + 3NO_2 + H_3O^+ + 2 H_2O$
 Varme artikler
Varme artikler
-
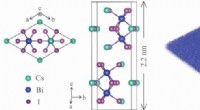 Odds er gode for unikke 2-D-forbindelserTil venstre, top- og sidebilleder af krystalstrukturerne af perovskit-afledt Cs3Bi2I9, et materiale syntetiseret ved Rice University, der viser valleytronics-kapaciteter. Hver enhedscelle indeholder t
Odds er gode for unikke 2-D-forbindelserTil venstre, top- og sidebilleder af krystalstrukturerne af perovskit-afledt Cs3Bi2I9, et materiale syntetiseret ved Rice University, der viser valleytronics-kapaciteter. Hver enhedscelle indeholder t -
 En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi
En naturinspireret belægning for at forhindre, at stoffer nedbrydes for tidligtForskere har udviklet en tynd belægning, der kan gøre det muligt for medicin at have færre tilsætningsstoffer. Kredit:Shutterstock.com Kemikere har udviklet en belægning, der kan gøre visse lægemi -
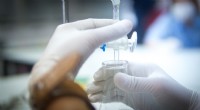 Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli
Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli -
 En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der
En lovende strategi til at øge aktiviteten i antimikrobielle peptiderKredit:Institut national de la recherche scientifique I en artikel offentliggjort for nylig i Plos One , forskere fra INRS-Institut Armand-Frappier Research Center rapporterede en strategi, der
- Hvilke fossile brændstof dannes under den mest ekstreme varme og tryk?
- Indien vejer forbud mod populært onlinespil efter dødsfald
- Hvilken form er DNA under interfase?
- Natrium- og kaliumbaserede batterier kan være nøglen til fremtidens smarte net
- Smeltende permafrost øger drivhusgasser fra arktiske søer
- Hvad er en måde at holde styr på energioverførsler ind og ud af jordsystemet?


