Beregning af atomer i en diamant:En simpel guide
* Diamanter er lavet af rent kulstof: Hver diamant er sammensat af kulstofatomer.
* Diamanter kommer i forskellige størrelser: En lille diamant vil have langt færre atomer end en stor diamant.
For at beregne antallet af atomer i en diamant skal du bruge:
1. Diamantens masse: Brug diamantens vægt i gram (g).
2. Molmassen af kulstof: Kulstof har en molær masse på 12,01 g/mol. Det betyder, at 12,01 gram kulstof indeholder 6,022 x 10^23 atomer (Avogadros tal).
3. En simpel beregning:
* Divider diamantens masse med den molære masse af kulstof for at finde antallet af mol kulstof.
* Gang antallet af mol med Avogadros tal for at finde det samlede antal atomer.
Eksempel:
Lad os sige, at du har en 1-karat diamant (0,2 gram).
1. Masse: 0,2 gram
2. Molar masse af kulstof: 12,01 g/mol
3. Beregning:
* Mol kulstof =0,2 g / 12,01 g/mol =0,0167 mol
* Antal atomer =0,0167 mol * 6,022 x 10^23 atomer/mol =1,01 x 10^22 atomer
Derfor indeholder en 1-karat diamant ca. 1,01 x 10^22 kulstofatomer.
 Varme artikler
Varme artikler
-
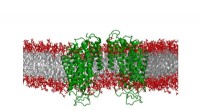 Opdagelse af en ny lægemiddelkandidat til at udvikle effektive behandlinger for hjernesygdommeProteinet NKCC1 er en transportør af ioner i hjernen; deres koncentration er afgørende for hjernens funktion. De nyopdagede forbindelser kan potent og selektivt blokere NKCC1, uden uønskede bivirkning
Opdagelse af en ny lægemiddelkandidat til at udvikle effektive behandlinger for hjernesygdommeProteinet NKCC1 er en transportør af ioner i hjernen; deres koncentration er afgørende for hjernens funktion. De nyopdagede forbindelser kan potent og selektivt blokere NKCC1, uden uønskede bivirkning -
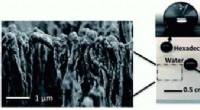 En skov af nanosvampestrukturer holder denne plast ren og pletfriKredit: Journal of Materials Chemistry A (2019). DOI:10.1039/C9TA01753D Teknologier som solpaneler og lysdioder kræver et dækmateriale, der afviser vand, snavs og olie, mens den stadig slipper ma
En skov af nanosvampestrukturer holder denne plast ren og pletfriKredit: Journal of Materials Chemistry A (2019). DOI:10.1039/C9TA01753D Teknologier som solpaneler og lysdioder kræver et dækmateriale, der afviser vand, snavs og olie, mens den stadig slipper ma -
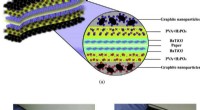 Formen på de kommende ting:Fleksibel, foldbare superkondensatorer til energilagring(a) skematisk af den symmetriske papirsuperkondensator med strukturen af GNPs elektroder (b) billede af den fremstillede superkondensator (c) billede af papirsuperkondensator i bøjetilstand. Kredit:
Formen på de kommende ting:Fleksibel, foldbare superkondensatorer til energilagring(a) skematisk af den symmetriske papirsuperkondensator med strukturen af GNPs elektroder (b) billede af den fremstillede superkondensator (c) billede af papirsuperkondensator i bøjetilstand. Kredit: -
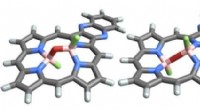 Opdagelse til at gruppere atomer påkalder PasteurForskernes molekyler ændrer form ved, at det centrale oxygenatom (vist med rødt) bøjer sig som et hængsel. De venstre og højre billeder viser, hvad formerne på disse molekyler er, når de er stabile. H
Opdagelse til at gruppere atomer påkalder PasteurForskernes molekyler ændrer form ved, at det centrale oxygenatom (vist med rødt) bøjer sig som et hængsel. De venstre og højre billeder viser, hvad formerne på disse molekyler er, når de er stabile. H
- Hvor mange atomer er der i svovl?
- Super lette dæmpere til lave toner
- Hvordan er celler organiseret i større og grupper for at hjælpe levende ting med at overleve?
- Hvad er farveændringen, når kobberoxid tilsættes brint?
- Hvor mange joules har en liter olie?
- Hvad er en optisk enhed, der producerer rigtige billeder?


