Den overraskende videnskab bag hvorfor appelsinskaljuice springer balloner
Den overraskende videnskab bag, hvorfor appelsinskaljuice springer balloner
Mange af os husker spændingen ved klasseværelseseksperimenter – ballondrevne biler, natron-vulkaner og den klassiske appelsinskal-og-ballontest, der viser, at en citrusskal kan få en ballon til at briste uden en skarp genstand. Disse enkle demonstrationer bringer abstrakt kemi ind i en levende hverdagsoplevelse.
Hvad har appelsinskal og balloner til fælles
Forskere ved Chemical Educational Xchange undersøgte mekanismen bag appelsinhud-tricket. Nøgleforbindelsen er limonen, et kulbrinte, der giver appelsiner deres karakteristiske duft. Limonen er ikke-polær, hvilket betyder, at dets kulstof- og brintatomer deler elektroner jævnt, hvilket ikke skaber nogen ladningsubalance.
Ballongummi er også et ikke-polært kulbrinte. Ifølge princippet om "lige opløses som" kan et ikke-polært opløsningsmiddel opløse et ikke-polært materiale. Når limonenolie kommer i kontakt med ballonens overflade, opløser den det ydre lag af gummiet, hvilket svækker strukturen og får ballonen til at springe. Holdet bekræftede dette ved at isolere limonen fra appelsinskaller og påføre det direkte på en ballon, hvilket gentog effekten i en YouTube-demonstration af Tommy Technetium.
Hvorfor nogle balloner modstår limonenangrebet
Ikke alle balloner er lige sårbare. Naturgummi indeholder lange isoprenkæder, der kan skilles, men mange kommercielle balloner er lavet af vulkaniseret gummi - et materiale, der er styrket af svovl-tværbindinger, der dramatisk øger sejheden. Infrarøde spektroskopiske undersøgelser viser, at de fleste fødselsdagsballoner er vulkaniserede, hvilket gør dem mere modstandsdygtige over for limonen. Vandballoner, som bruger ikke-vulkaniseret gummi, er meget mere skrøbelige og springer let, når de udsættes for appelsinskaljuice. Citroner, som også indeholder limonen, kan give samme effekt.
Disse resultater fremhæver, hvordan subtile kemiske egenskaber styrer hverdagens fænomener og tilbyder en håndgribelig lektion i kraften ved ikke-polære interaktioner.
 Varme artikler
Varme artikler
-
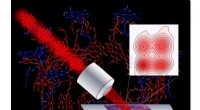 Forskere udvikler mikroskop til at spore lysenergistrøm i fotosyntetiske cellerAnvender en række ultrakorte laserpulser, et nyt mikroskop afslører indviklede detaljer, der styrer fotosyntetiske processer i lilla bakterier. Kredit:Vivek Tiwari, Yassel Acosta og Jennifer Ogilvie
Forskere udvikler mikroskop til at spore lysenergistrøm i fotosyntetiske cellerAnvender en række ultrakorte laserpulser, et nyt mikroskop afslører indviklede detaljer, der styrer fotosyntetiske processer i lilla bakterier. Kredit:Vivek Tiwari, Yassel Acosta og Jennifer Ogilvie -
 Teknologi i laboratorieskala genbruger spildevand til brint til brug i brændstofproduktionAlex Lewis, en ph.d.-studerende ved Bredesen Center for Tværfaglig Forskning og Uddannelse, prøver en mikrobiel elektrolysecelle for at måle brint- og protonkoncentrationer. Kredit:Oak Ridge National
Teknologi i laboratorieskala genbruger spildevand til brint til brug i brændstofproduktionAlex Lewis, en ph.d.-studerende ved Bredesen Center for Tværfaglig Forskning og Uddannelse, prøver en mikrobiel elektrolysecelle for at måle brint- og protonkoncentrationer. Kredit:Oak Ridge National -
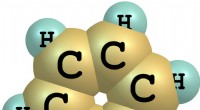 Hvordan benzen produceres fra råolie og relaterede processerAf Eric Bank, MBA, MS Finance Opdateret 24. marts 2022 Benzen (C6 H6 ) er det enkleste aromatiske kulbrinte. Dens plane ring med seks carbonatomer deler delokaliserede elektroner, hvilket giver den
Hvordan benzen produceres fra råolie og relaterede processerAf Eric Bank, MBA, MS Finance Opdateret 24. marts 2022 Benzen (C6 H6 ) er det enkleste aromatiske kulbrinte. Dens plane ring med seks carbonatomer deler delokaliserede elektroner, hvilket giver den -
 Makerspaces kunne muliggøre udbredt anvendelse af mikrofluidikMikrofluidiske enheder til at udføre forskellige assays blev skabt med værktøjerne i Lincoln Laboratorys Technology Office Innovation Laboratory. Kredit:Nicole Fandel I mere end et årti, videnskab
Makerspaces kunne muliggøre udbredt anvendelse af mikrofluidikMikrofluidiske enheder til at udføre forskellige assays blev skabt med værktøjerne i Lincoln Laboratorys Technology Office Innovation Laboratory. Kredit:Nicole Fandel I mere end et årti, videnskab
- Sådan forenkles radikale fraktioner
- Hvilken af objekterne har mest tyngdekraft en sandkornmarmorbowlingkugle eller tennisbold?
- Hvad sker der med klimaet, hvis du bevæger dig nordpå i breddegrad?
- Hvis en person har masse af 60 kg og hastigheden på 2ms, hvad er det i størrelsesordenen denne mom…
- Rusland begynder at tilbyde rumvandringer for turister
- Hvad gør kemisk forvitring to klipper?


