Beregning af masseprocent:En trin-for-trin guide
Af Oxana Fox • 29. april 2023 kl. 12.10 EST
Hvad er masseprocent?
Masseprocent udtrykker koncentrationen af et opløst stof i forhold til den samlede masse af en opløsning. Det beregnes som en procentdel af det opløste stofs masse divideret med massen af hele opløsningen.
Masseprocentformlen
For at bestemme masseprocentens sammensætning af en forbindelse i en blanding, brug:
Mass Percent =\(\frac{a}{M} \time 100\)hvor a er massen af det opløste stof og M er opløsningens samlede masse (opløst stof + opløsningsmiddel).
Eksempel:Beregning af masseprocent
Antag, at 10 g natriumchlorid (NaCl) og 6 g natriumbicarbonat (NaHCO₃) opløses i 120 g vand. Den samlede opløsningsmasse er:
\(M =10\text{ g} + 6\text{ g} + 120\text{ g} =136\text{ g}\)
Masseprocent af NaCl:
\(\frac{10\text{ g}}{136\text{ g}} \times 100\% =7,35\%\)
Masseprocent af NaHC03:
\(\frac{6\text{ g}}{136\text{ g}} \time 100\% =4,41\%\)
Hvorfor masseprocent betyder noget
Masseprocent giver kemikere mulighed for at kvantificere de relative bidrag fra hver komponent i en blanding, hvilket hjælper med reaktionsdesign, kvalitetskontrol og analytiske beregninger. For eksempel at bestemme grundstofsammensætningen af glucose eller koncentrationen af opløste stoffer i farmaceutiske formuleringer.
Forbindelse til Molar Masse
Molær masse, massen af et mol af et stof, er relateret til masseprocent ved omregning mellem masse- og molmængder:
M =\(\frac{m}{n}\)
hvor M er den molære masse (kgmol⁻¹), m er stoffets masse, og n er antallet af mol.
TL;DR
En mol er lig med Avogadros antal atomer eller molekyler. Mens antallet af partikler er det samme for ethvert grundstof, er massen forskellig, fordi hvert atom har en særskilt atomvægt.
 Varme artikler
Varme artikler
-
 Biologi og kemi kombineres for at generere nye antibiotikaFrugtlegemer fra svampen Clitopilus passeckerianus genereret i laboratoriet. Kredit:University of Bristol Kombinerer innovationerne inden for syntetisk biologi med biologi og kemi, et team af vi
Biologi og kemi kombineres for at generere nye antibiotikaFrugtlegemer fra svampen Clitopilus passeckerianus genereret i laboratoriet. Kredit:University of Bristol Kombinerer innovationerne inden for syntetisk biologi med biologi og kemi, et team af vi -
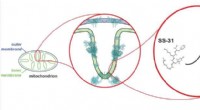 Forskere udforsker potentiel behandling for mitokondriesygdommeEt diagram, der viser SS-31, et peptid, eller kort kæde af aminosyrer, der let trænger ind i kroppens celler. SS-31 bliver støvet op af mitokondrier og smyger sig ind mod de indre vægge, hvor det skær
Forskere udforsker potentiel behandling for mitokondriesygdommeEt diagram, der viser SS-31, et peptid, eller kort kæde af aminosyrer, der let trænger ind i kroppens celler. SS-31 bliver støvet op af mitokondrier og smyger sig ind mod de indre vægge, hvor det skær -
 Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi
Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi -
 Hvor længe holder hukommelsen? Til formhukommelseslegeringer, jo længere jo bedreKredit:CC0 Public Domain Kendt for mange som muskeltråd eller memory metal, formhukommelseslegeringer er materialer, der kan bøjes eller deformeres, og derefter vende tilbage til deres oprindelige
Hvor længe holder hukommelsen? Til formhukommelseslegeringer, jo længere jo bedreKredit:CC0 Public Domain Kendt for mange som muskeltråd eller memory metal, formhukommelseslegeringer er materialer, der kan bøjes eller deformeres, og derefter vende tilbage til deres oprindelige


