Beregning af graden af umættethed:En trin-for-trin guide
Af Allan Robinson | Opdateret 30. august 2022
Billede udlånt af SDI Productions/E+/GettyImages
Trin 1
Begynd med den generelle formel for graden af umættethed (DU):
DU = 1 + \displaystyle\sum\frac{n_i(v_i-2)}{2}
hvor n_i er antallet af atomer af typen i og v_i er dens valens. Dette udtryk fungerer for enhver molekylær formel.
Trin 2
Identificer valensen for de fælles elementer:Carbon (4), Nitrogen (3), Ilt (2), Hydrogen og halogener (1). Disse værdier er standard i organisk kemi.
Trin 3
Erstat valenserne i formlen og forenkle hvert led:
- Kulstof: n₄(4–2)/2 = n₄
- Nitrogen: n₃(3–2)/2 = n₃/2
- Oxygen: n₂(2–2)/2 = 0
- Brint/halogener: n₁(1–2)/2 = –n₁/2
Trin 4
Indsæt de forenklede udtryk tilbage i det overordnede udtryk:
DU = 1 + (–n₁/2) + 0 + (n₃/2) + n₄ = 1 – n₁/2 + n₃/2 + n₄
Her n₁ tæller brint og halogener, n₃ tæller nitrogen og n₄ tæller kulstof.
Trin 5
Genudtryk formlen i en mere bekvem form for molekyler, der kun indeholder disse elementer:
DU = 1 + C + (N – X)/2
hvor C , N og X er antallet af henholdsvis carbon-, nitrogen- og halogen/hydrogen-atomer. Denne kompakte ligning tillader hurtig beregning af umættethed for de fleste organiske forbindelser.
Ved hjælp af denne metode kan kemikere forudsige strukturelle træk – ringe, dobbeltbindinger og tredobbelte bindinger – før de bekræfter dem med spektroskopiske teknikker.
 Varme artikler
Varme artikler
-
 Forskere bruger nye datavidenskabelige værktøjer til at fange enkeltmolekyler i aktionEt molekyle, hvis sti sporet i tid er vist med den blå linje, lejlighedsvis vandrer ind i et stærkt oplyst grønt område. Inden for denne region, molekylet er ophidset og begynder at udsende lys med en
Forskere bruger nye datavidenskabelige værktøjer til at fange enkeltmolekyler i aktionEt molekyle, hvis sti sporet i tid er vist med den blå linje, lejlighedsvis vandrer ind i et stærkt oplyst grønt område. Inden for denne region, molekylet er ophidset og begynder at udsende lys med en -
 Fentanyl kan gøre first responders syge. Her er en mulig løsningEn dødelig dosis heroin sammenlignet med en dødelig dosis fentanyl. Dette er kun en illustration - stoffet, der faktisk er vist på dette billede, er et kunstigt sødestof. Kredit:© Bruce A. Taylor/NH S
Fentanyl kan gøre first responders syge. Her er en mulig løsningEn dødelig dosis heroin sammenlignet med en dødelig dosis fentanyl. Dette er kun en illustration - stoffet, der faktisk er vist på dette billede, er et kunstigt sødestof. Kredit:© Bruce A. Taylor/NH S -
 Afsætning af jernarter inde i ZSM-5 for at oxidere cyclohexan til cyclohexanonKredit:Unsplash/CC0 Public Domain Den direkte katalytiske oxidation af alkaner har høj atomøkonomi og anvendelsesværdi til dannelse af tilsvarende kemiske organiske produkter, såsom alkoholer, ald
Afsætning af jernarter inde i ZSM-5 for at oxidere cyclohexan til cyclohexanonKredit:Unsplash/CC0 Public Domain Den direkte katalytiske oxidation af alkaner har høj atomøkonomi og anvendelsesværdi til dannelse af tilsvarende kemiske organiske produkter, såsom alkoholer, ald -
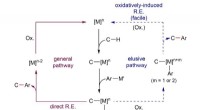 Forskere opnår arylering af CH-bindinger under milde forholdOxidation af metallet (M, iridium, blå vej) fører til et fald på 19 kcal/mol i reaktionens energibarriere, og tillader aryleringen at ske ved stuetemperatur. Kredit:Institut for Grundvidenskab Car
Forskere opnår arylering af CH-bindinger under milde forholdOxidation af metallet (M, iridium, blå vej) fører til et fald på 19 kcal/mol i reaktionens energibarriere, og tillader aryleringen at ske ved stuetemperatur. Kredit:Institut for Grundvidenskab Car
- Vil et objekt med en masse på 0,33n flyde?
- Kan du se Jupiter fra Wales?
- Hvad er molariteten af en 3,45L -opløsning, der indeholder 0,491 mol natriumsulfat?
- Hvilket får mediet til at vibrere i en retning parallel bølgebevægelse?
- To eksempler på, hvordan Nilen formede det gamle Egypten
- Fagocytter:Din krops nøgleforsvar mod infektion


