Hvordan temperatur, pH og substratniveauer former enzymydelsen
Creatas/Creatas/Getty Images
Enzymer er specialiserede proteiner, der vedtager præcise tredimensionelle strukturer, hvilket gør dem i stand til at katalysere biokemiske reaktioner med bemærkelsesværdig hastighed. Effektiviteten af et enzym er styret af flere kritiske miljøvariabler, primært temperatur, pH og substratkoncentration.
Temperatur
Enzymaktivitet stiger med temperaturen, fordi den kinetiske energi øges, hvilket fører til hyppigere kollisioner mellem enzym og substrat. Humane enzymer når maksimal aktivitet omkring 37°C (98.6°F), hvilket falder sammen med normal kropstemperatur. Ud over dette optimum begynder proteiner at denaturere:hydrogenbindinger og hydrofobe interaktioner brydes, hvilket ændrer enzymets konformation og formindsker den katalytiske funktion.
pH
Hvert enzym har et optimalt pH-område, der afspejler surhedsgraden eller alkaliniteten i dets naturlige miljø. Afvigelser fra dette optimale destabiliserer enzymets struktur - svarende til termisk denaturering - reducerende aktivitet. Menneskelige fysiologiske væsker er typisk tæt på pH7,2, hvilket gør denne værdi til den ideelle tilstand for de fleste kropsenzymer.
Substratkoncentration
Fordi et enzym kun kan binde ét substratmolekyle ad gangen, afhænger dets omsætningshastighed af, hvor mange substratmolekyler der er tilgængelige. Ved lave koncentrationer øger stigende substratniveauer aktiviteten, efterhånden som flere bindingshændelser forekommer. Når alle aktive steder er besat, vil reaktionshastigheden plateauer, hvilket afspejler enzymmætning. Dette forhold beskrives ofte af Michaelis-Menten-ligningen.
Enzymkoncentration
Når substratforsyningen er rigelig, øger en stigning i koncentrationen af enzym direkte antallet af katalytiske steder, hvilket giver en lineær stigning i reaktionshastigheden. Denne proportionalitet understreger, hvorfor celler regulerer enzymsyntese som reaktion på metaboliske krav.
Forståelse af disse variabler er afgørende for områder lige fra lægemiddeludvikling til industriel biokatalyse, hvor præcis kontrol over reaktionsbetingelser kan optimere udbytte og effektivitet.
 Varme artikler
Varme artikler
-
 Potentielt alternativ til petroleumspolycarbonat indeholdende miljøhormonkilderBio-polycarbonatet er meget gennemsigtigt, som tropiske fisk kan ses igennem. Kredit:Kredit:Korea Research Institute of Chemical Technology (KRICT) Korea Research Institute of Chemical Technology
Potentielt alternativ til petroleumspolycarbonat indeholdende miljøhormonkilderBio-polycarbonatet er meget gennemsigtigt, som tropiske fisk kan ses igennem. Kredit:Kredit:Korea Research Institute of Chemical Technology (KRICT) Korea Research Institute of Chemical Technology -
 Biosensorteknologier til at tilbyde mere effektive tilgange til sygdomsbehandlingMonash Biomedicine Discovery Institutes professor Mibel Aguilar og Dr. John Lee ved siden af den nyudviklede biosensorteknologi. Kredit:Steve Morton Hver celle i vores kroppe er formet af dens y
Biosensorteknologier til at tilbyde mere effektive tilgange til sygdomsbehandlingMonash Biomedicine Discovery Institutes professor Mibel Aguilar og Dr. John Lee ved siden af den nyudviklede biosensorteknologi. Kredit:Steve Morton Hver celle i vores kroppe er formet af dens y -
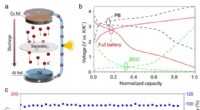 Konstruktion af kulstofbaserede celle-lignende kugler til robust kaliumanode(a) Skematisk illustration af K-ion-fuldbatteriet baseret på det forberedte BCC og Preussisk blå (PB). (b) Opladningsafladningsprofiler for halvbatteriet og fuldt batteri. (c) Cykelstabilitet ved 500
Konstruktion af kulstofbaserede celle-lignende kugler til robust kaliumanode(a) Skematisk illustration af K-ion-fuldbatteriet baseret på det forberedte BCC og Preussisk blå (PB). (b) Opladningsafladningsprofiler for halvbatteriet og fuldt batteri. (c) Cykelstabilitet ved 500 -
 Miljøpåvirkning af frostvæske:Virkninger på dyreliv, planter og jordHvad er frostvæske? Frostvæske er en væske, der sænker vandets frysepunkt og beskytter motorens kølesystemer mod frostskader og overkogning. Det er typisk en blanding af vand og en glykol, sædvanligv
Miljøpåvirkning af frostvæske:Virkninger på dyreliv, planter og jordHvad er frostvæske? Frostvæske er en væske, der sænker vandets frysepunkt og beskytter motorens kølesystemer mod frostskader og overkogning. Det er typisk en blanding af vand og en glykol, sædvanligv
- Hvad er den nuværende accepterede Hubble konstant værdi i kosmologi?
- Hvordan er en celle som en fabrik?
- Studer i udlandet for pendlere:et casestudie ved University of New Hampshire i Manchester
- Hvad er biofotografer?
- Gasdynamik i et nærliggende protostellart binært system studeret med ALMA
- Hvordan bruger et ur elastisk energi?


