Forstå grundstofklassificering i det periodiske system
Af Mary MacIntosh Opdateret 30. august 2022
Det periodiske system er hjørnestenen i kemi, der katalogiserer alle kendte kemiske grundstoffer - fra naturligt forekommende arter til syntetiske kreationer. Dets moderne arrangement, som blev udviklet af den russiske kemiker Dmitri Mendeleev i 1869, placerer elementer i et gitter defineret af atomnummer snarere end den ældre atomvægt-rækkefølge.
Periodisk organisation
I dette layout indtager hvert element en unik position ved skæringspunktet mellem en lodret gruppe (søjle) og en vandret periode (række). De syv perioder svarer til successive elektronskaludvidelser, mens de 18 grupper afspejler delte valens-elektronkonfigurationer, der driver analog kemisk adfærd.
Videnskabelig begrundelse
I hjertet af hvert grundstof ligger et atom:en positivt ladet kerne omgivet af en sky af elektroner. Antallet af protoner - dets atomnummer - bestemmer elementets identitet. Elektroner befolker diskrete skaller; den yderste, eller valens, skal dikterer, hvordan et element reagerer. Grundstoffer inden for samme gruppe har identiske valens-elektrontal, hvilket forklarer deres parallelle reaktivitetsmønstre. Når man krydser en periode fra venstre mod højre, fyldes valensskaller sekventielt, hvilket tegner sig for den gradvise ændring i egenskaber.
Alkali- og jordalkalimetaller
Yderst til venstre på bordet sidder de meget reaktive alkalimetaller (Gruppe1) og ved siden af dem de lidt mindre reaktive jordalkalimetaller (Gruppe2). Bortset fra brint besidder alkalimetaller en enkelt valenselektron, der let doneres, hvilket gør dem eksplosive i luft eller vand. Alkaliske jordmetaller med to valenselektroner er noget hårdere, men findes stadig sjældent i deres grundstofform i naturen.
Overgangsmetaller
Den centrale region af diagrammet (Gruppe 3-12) er domineret af overgangsmetaller. Disse elementer er faste ved stuetemperatur - kviksølv er den eneste væske - udviser metallisk glans og er formbare. Deres delvist fyldte d‑orbitaler tillader en række oxidationstilstande, hvilket gør dem alsidige inden for katalyse og materialevidenskab. Lanthanid- og actinid-serien, der repræsenterer f-elektronfyldning, vises traditionelt under hovedtabellen.
Metalloider og ikke-metaller
En diagonal grænse adskiller den metalliske blok fra den ikke-metalliske blok. Metalloider såsom germanium og arsen, placeret langs denne linje, udviser mellemliggende egenskaber. Til højre ligger ikke-metallerne:fra gasser som brint og nitrogen til elementer som oxygen og fluor. Disse arter har typisk høj elektronegativitet og har tendens til at få elektroner for at opnå fuld valensskaller.
Ædelgasser
Gruppe18 er vært for ædelgasserne - helium, neon, argon, krypton, xenon og radon. Deres ydre skaller er komplette, hvilket giver dem ekstrem kemisk inertitet. Følgelig forbliver de næsten udelukkende i elementær form og fremstår som farveløse, lugtløse gasser ved standardtemperatur og -tryk.
 Varme artikler
Varme artikler
-
 Indestår for Vonnegut:Ingeniører studerer polymer, der fryser ved stuetemperaturNår det blandes med en præcis mængde vand, polymeren størkner til en blød pasta ved stuetemperatur. Kredit:Swanson School of Engineering/Sachin Velankar I Kurt Vonneguts sci-fi-klassiker Kattens
Indestår for Vonnegut:Ingeniører studerer polymer, der fryser ved stuetemperaturNår det blandes med en præcis mængde vand, polymeren størkner til en blød pasta ved stuetemperatur. Kredit:Swanson School of Engineering/Sachin Velankar I Kurt Vonneguts sci-fi-klassiker Kattens -
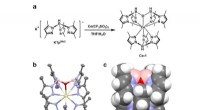 Dybblå organiske lysemitterende dioder baseret på et dublet-emission cerium(III) kompleksen. Syntetisk rute for komplekset. b. Enkeltkrystalstruktur af komplekset vist som ellipsoider ved 50 % sandsynlighedsniveau, hvor gul repræsenterer Ce, pink repræsenterer B, blå repræsenterer N, rød
Dybblå organiske lysemitterende dioder baseret på et dublet-emission cerium(III) kompleksen. Syntetisk rute for komplekset. b. Enkeltkrystalstruktur af komplekset vist som ellipsoider ved 50 % sandsynlighedsniveau, hvor gul repræsenterer Ce, pink repræsenterer B, blå repræsenterer N, rød -
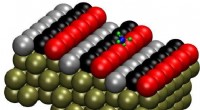 Lokalisering af den præcise reaktionsvej:Metan-dissociation på platinPt(211)-overfladen har tre-atom-brede terrasser og et-atom-høje trin. Forskerne mærkede rækken af atomer på trinkanten som trin (rød), den midterste række som terrasse (sort) og den sidste række som
Lokalisering af den præcise reaktionsvej:Metan-dissociation på platinPt(211)-overfladen har tre-atom-brede terrasser og et-atom-høje trin. Forskerne mærkede rækken af atomer på trinkanten som trin (rød), den midterste række som terrasse (sort) og den sidste række som -
 Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
- Hvordan beviste Louis Pasteur sin kimteori om sygdom?
- Når kobber II hydroxid og natriumnitrat opvarmes?
- Hvad er det at være en bidronning?
- Hvorfor faldt nedbøren over det asiatiske indre plateau-område pludseligt omkring 1999?
- Ny skræddersyet nanoferroelektrisk fra byggesten
- Hvad er solspotcyklussen?


