Konvertering af millimoler til milligram:en praktisk vejledning
Af Sean Lancaster
Opdateret 30. august 2022
Ivan-balvan/iStock/GettyImages
I laboratoriemiljøer er kemiske mængder typisk udtrykt i gram. Reaktionsstøkiometri kræver dog mol - en enhed, der repræsenterer et fast antal molekyler (Avogadros konstant, 6,02×10²³). For at bestemme massen svarende til et bestemt antal mol, skal du først kende forbindelsens formelvægt.
Trin 1:Find formelvægten
Beregn formelvægten ved at summere atomvægtene af alle atomer i molekylformlen. Atomvægtene er opført på NIST periodiske system eller ethvert standard periodisk system.
Eksempel – Jern(III)oxid (rust):Fe₂O₃
- Atomvægt af Fe:55,845 gmol⁻¹
- Atomvægt af O:16.000 gmol⁻¹
Formelvægt =2×55,845+3×16,000=111,69+48,00=159,69gmol⁻¹ (massen af et mol Fe₂O3).
Trin 2:Konverter til Millimoles
En millimol er lig med en tusindedel af en mol. Divider formlens vægt med 1.000.
1 molFe2O3=159,69g → 1mmolFe2O3=159,69g/1.000=0,1597g=159,69mg.
Trin 3:Beregn den påkrævede masse
Gang de ønskede millimol med massen pr. millimol.
Eksempel:15mmolFe₂O₃ nødvendig → 15×159,69mg=2.395,35mg Fe₂O3.
Hvad du skal bruge
- Adgang til et pålideligt periodisk system (f.eks. NIST)
- Videnskabelig lommeregner eller regneark
 Varme artikler
Varme artikler
-
 Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ
Forskere udvikler semi-flydende metalanode til næste generations batterierCarnegie Mellon-forskere har udviklet en dobbeltledende polymer/carbon-kompositmatrix med lithiummikropartikler, der kan bruges som elektrode i næste generations batterier. Kredit:Carnegie Mellon Univ -
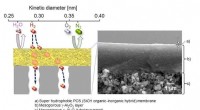 Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve
Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve -
 Forskere opdager forviklinger af serotoninreceptorer, der er afgørende for bedre behandlingLægemidler varierer i deres evne til at aktivere 5-HT2B serotoninreceptoren. Nogle lægemidler (RØD) aktiverer kraftigt receptoren og forårsager potentielt livstruende hjerteklapsygdomme, mens andre ku
Forskere opdager forviklinger af serotoninreceptorer, der er afgørende for bedre behandlingLægemidler varierer i deres evne til at aktivere 5-HT2B serotoninreceptoren. Nogle lægemidler (RØD) aktiverer kraftigt receptoren og forårsager potentielt livstruende hjerteklapsygdomme, mens andre ku -
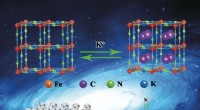 Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis
Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis
- Når et stof går fra fast til flydende tilstand uden ændring i temperatur, kaldes den varme, der t…
- Skrive noter på din TI-84 Silver Edition lommeregner:En trin-for-trin guide
- Indfangning af små partikler:Et alsidigt værktøj til nanomanipulation
- Hvorfor er der ingen mekaniske bølger i OutSpace?
- Hvad er nulpunkts celsius skalaen?
- Hvornår blev solen aldrig skinnet den dag skabt?


