Mestring af balancen mellem redoxligninger:En trin-for-trin-vejledning
Af Jack Brubaker | Opdateret 30. august 2022
vidalidali/iStock/GettyImages
Oxidationsreduktion, eller "redox", reaktioner er en hjørnesten i kemiske transformationer. De involverer overførsel af elektroner mellem arter:tabte elektroner oxideres, de opnåede elektroner reduceres. Balancering af en kemisk ligning sikrer, at hvert atom og hver ladning vises på begge sider, og ære bevarelsen af masse og ladning - grundlæggende principper i termodynamikkens første lov. Redox-reaktioner tager dette et skridt videre ved også at balancere elektronantallet.
Trin 1:Identificer oxidation og reduktion
Skriv den ubalancerede reaktion og bestem, hvilke atomer der ændrer oxidationstilstand. For eksempel i den sure reaktion:
MnO4 – + C2 O4 2– + H + → Mn 2+ + CO2 + H2 O
Fordi oxygen næsten altid bærer en ladning -2, er den samlede ladning -1 af MnO4 – tvinger mangan til at have en +7 oxidationstilstand. I C2 O4 2– , hvert kulstof er +3. Efter reaktionen er Mn +2 og kulstof +4—mangan reduceres, kulstof oxideres.
Trin 2:Skriv halvreaktioner med elektroner
Udtryk oxidationen og reduktionen som separate halvreaktioner, og tilføj elektroner for at balancere ladningen:
Reduktion: MnO4 – + 8 H + + 5 e – → Mn 2+ + 4 H2 O
Oxidation: C2 O4 2– → 2 CO2 + 2 e –
Trin 3:Udlign elektronoverførsel
Skaler halvreaktionerne, så elektronantallet stemmer overens. Reduktionstrinnet kræver 5 elektroner; kun oxidationstrinnet 2. Gang reduktionen med 2 og oxidationen med 5:
2 MnO4 – + 16 H + + 10 e – → 2 Mn 2+ + 8 H2 O
5 C2 O4 2– → 10 CO2 + 10 e –
Trin 4:Kombiner og annuller
Tilføjelse af de to afbalancerede halvreaktioner annullerer elektronerne:
2 MnO4 – + 16 H + + 5 C2 O4 2– → 2 Mn 2+ + 8 H2 O + 10 CO2
Dette er den fuldt afbalancerede redoxligning.
Ved at følge disse systematiske trin kan du trygt afbalancere enhver redoxreaktion, uanset om det er i laboratoriemiljøer eller akademiske kurser.
 Varme artikler
Varme artikler
-
 Stive, ømme knæ? Lab-fremstillet bruskgelé overgår den ægte vareEt hydrogel-baseret implantat kunne erstatte slidt brusk og lindre knæsmerter uden at erstatte hele leddet. Kredit:Benjamin Wiley, Duke University. Smertestillende midler i håndkøb, fysioterapi, st
Stive, ømme knæ? Lab-fremstillet bruskgelé overgår den ægte vareEt hydrogel-baseret implantat kunne erstatte slidt brusk og lindre knæsmerter uden at erstatte hele leddet. Kredit:Benjamin Wiley, Duke University. Smertestillende midler i håndkøb, fysioterapi, st -
 Forskere opdager, hvordan overflader kan have hjulpet tidligt liv på Jorden med at begyndeSpontant dannede protoceller, som ligner balloner forankret til en overflade af et netværk af reb, visualiseres ved 3D konfokal mikroskopi. Kredit:Irep Gözen På den tidlige jord, en række spontane
Forskere opdager, hvordan overflader kan have hjulpet tidligt liv på Jorden med at begyndeSpontant dannede protoceller, som ligner balloner forankret til en overflade af et netværk af reb, visualiseres ved 3D konfokal mikroskopi. Kredit:Irep Gözen På den tidlige jord, en række spontane -
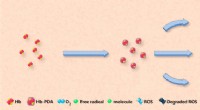 Fremstilling af kunstigt blod til transfusionerKredit:American Chemical Society Blodtransfusioner kan redde livet for patienter, der har lidt stort blodtab, men hospitaler har ikke altid nok eller den rigtige type ved hånden. På jagt efter en
Fremstilling af kunstigt blod til transfusionerKredit:American Chemical Society Blodtransfusioner kan redde livet for patienter, der har lidt stort blodtab, men hospitaler har ikke altid nok eller den rigtige type ved hånden. På jagt efter en -
 Oxidsintring ved lufttrykskontrolOpstilling af en prøve i en lufttryksreguleringsatmosfæreovn. Kredit:Toyohashi University of Technology Professor Hiromi Nakano fra Toyohashi University of Technology har samarbejdet med en virkso
Oxidsintring ved lufttrykskontrolOpstilling af en prøve i en lufttryksreguleringsatmosfæreovn. Kredit:Toyohashi University of Technology Professor Hiromi Nakano fra Toyohashi University of Technology har samarbejdet med en virkso


